781
25 Марта 2021
Шан Ли, Сергей Р. Константинов, Рон Смитс, Майкель П. Пеппеленбош
Одним из значимых факторов в инициации и развитии колоректального рака (КРР) является кишечная микробиота. В настоящее время существует распространенное мнение о бактериальном онкогенезе, который заключается в том, что КРР запускается локальной колонизацией слизистой оболочки специфическими патогенными микроорганизмами и что последующие изменения в перитуморозной зоне допускают колонизацию среды оппортунистическими микробами, что еще больше способствует прогрессированию заболевания. Таким образом, скрининг КРР по бактериал...
Одним из значимых факторов в инициации и развитии колоректального рака (КРР) является кишечная микробиота. В настоящее время существует распространенное мнение о бактериальном онкогенезе, который заключается в том, что КРР запускается локальной колонизацией слизистой оболочки специфическими патогенными микроорганизмами и что последующие изменения в перитуморозной зоне допускают колонизацию среды оппортунистическими микробами, что еще больше способствует прогрессированию заболевания. Таким образом, скрининг КРР по бактериал...
Шан Ли, Сергей Р. Константинов, Рон Смитс, Майкель П. Пеппеленбош
Одним из значимых факторов в инициации и развитии колоректального рака (КРР) является кишечная микробиота. В настоящее время существует распространенное мнение о бактериальном онкогенезе, который заключается в том, что КРР запускается локальной колонизацией слизистой оболочки специфическими патогенными микроорганизмами и что последующие изменения в перитуморозной зоне допускают колонизацию среды оппортунистическими микробами, что еще больше способствует прогрессированию заболевания. Таким образом, скрининг КРР по бактериальной модели «водитель-пассажир» позволяет провести раннюю диагностику КРР или помочь в выборе превентивного вмешательства. Такие попытки в настоящее время аргументируются тем, что для инициирования и развития КРР требуется организация бактериальных сообществ, называемых биопленками. Здесь мы исследуем концепцию, согласно которой полимикробная биопленка способствует проканцерогенной активности.
Тенденции
Нигде в организме человека микробиом не проявляет свою активностьтак ярко и четко как в желудочно-кишечном тракте (ЖКТ). Здесь обитает около 40 триллионов микробов, представляющих как минимум 1000 видов, подавляющее большинство которых находится в толстой кишке [1]. Таким образом, следует ожидать, что, если микробиом и патофизиология человека взаимосвязаны, это должно быть особенно выражено в толстой кишке. Основная роль микробиома в патофизиологии острых и хронических воспалительных заболеваний толстой кишки действительно хорошо известна [2, 3]. Интересно, что, несмотря на относительно незначительную бактериальную колонизацию желудка, связь между раком желудка и инфекцией Helicobacter pylori не подвергается сомнению. Появляются свидетельства того, что другие микробиоты, колонизирующие желудок, также могут быть задействованы в прогрессировании рака желудка у человека [4, 5]. Причинно-следственная связь между колоректальным раком (КРР) и микробиомом была менее очевидной, однако в последнее время и в этом направлении ученые продвинулись вперед, связав кишечную микробиоту с прогрессированием КРР [6–13]. Такие исследования породили большие надежды на то, что скрининг микробиологических компонентов может обеспечить раннюю диагностику КРР или что заболевание можно потенциально предотвратить с помощью диеты или других вмешательств, которые могут модулировать состав микробиома толстой кишки. Ввиду существенной проблемы КРР в современном обществе такие усилия очень важны [14, 15].
В настоящее время становится ясно, что КРР не зависит от одного конкретного патогенного микроорганизма – на него влияет сложное кишечное бактериальное сообщество. Исследования, сравнивающие анализы кала у пациентов, больных КРР, и относительно здоровых контрольных образцов, продемонстрировали существенные различия в составе их кишечного микробиома [16, 17]. Эти исследования также показывают, что КРР характеризуется микробным дисбиозом [12, 18]. Кроме того, недавние исследования показали, что мыши с дефицитом в иммунном сенсоре Aim2, которые были колонизированы дисбактериальной кишечной микробиотой, стали очень чувствительны к онкогенезу в толстой кишке по сравнению с теми же мышами, колонизированными здоровой микробиотой [19]. Важные вопросы в этой области включают степень, когда эти изменения являются причиной или следствием КРР, в дополнение к выявлению механизмов, опосредующих такие изменения. В настоящее время разрабатываются различные модели бактериального канцерогенеза, что позволяет предположить, как кишечная микробиота, а также взаимодействия микроб-микроб и микроб-хозяин вносят вклад в развитие КРР [20–22]. Тем не менее, механизмы, посредством которых кишечная микробиота взаимодействует с самой собой и человеком-хозяином, вызывая инициацию и прогрессирование КРР, остаются в значительной степени неясными. Становится понятно, что взаимодействия, вызывающие КРР, сильно зависят от природы и пространственной организации мультивидовых бактериальных сообществ в структурах более высокого порядка (так называемых биопленках) [11, 13]. В этой статье мы утверждаем, что полимикробные биопленки способствуют проканцерогенной активности, и что инвазивная биопленка, по-видимому, является необходимой для инициации КРР.
От одного патогенного микроорганизма к полимикробным инфекциям и онкологии
Специфические микроорганизмы сами по себе способны вызывать канцерогенные и другие опухолевые процессы в желудочно-кишечном тракте человека (что очевидно в случае с H. pylori при раке желудка) [23–26]. Кроме того, и другие опухолевые процессы могут быть спровоцированы определенным патогеном, например, рак печени при хроническом вирусном гепатите B или C, рак шейки матки при вирусе папилломы человека, лимфома Беркитта при вирусе Эпштейна-Барр и рак мочевого пузыря, индуцируемый Schistosoma haematobium [20, 21, 27, 28].
Что касается КРР, в двух исследованиях, проведенных в Северной Америке в 2012 году, было обнаружено большое скопление Fusobacterium nucleatum в опухолевой ткани КРР по сравнению с окружающей нормальной тканью [7, 9]. Удалось установить что эта бактерия связана с развитием КРР, о чем свидетельствует ее способность проникать в слизистую оболочку толстой кишки, вызывать местное воспаление и повышенную экспрессию таких цитокинов, как интерлейкин 6 (ИЛ-6), ИЛ-8, ИЛ-12, трансформирующий фактор роста бета (TGF-b) и фактор некроза опухоли (ФНО), и тем самым потенциально усугублять КРР [10, 29, 30]. Бактериальная инфекция F. nucleatum напрямую способствует колоректальному канцерогенезу, о чем свидетельствуют два недавних исследования с использованием мышиной модели ApcMin / + и клеточных линий КРР человека - данные показывают, что инвазия F. nucleatum приводит к рекрутированию инфильтрирующих опухоль иммунных клеток CD11b + (интегрин-субъединица / M, ITGAM) в толстой кишке и созданию онкогенной / провоспалительной микросреды [10, 31]. Более того, данный процесс рекрутирования, по-видимому, зависит от бактериальной адгезии, опосредованной FadA (деградацией адгезиновых жирных кислот A) [10, 31]. Ранее было показано, что FadA связывается с эпителиальным кадгерином (E-cadherin; или кадгерин 1, CDH1), что приводит к активации передачи сигналов b-катенина [31]. Что касается F. nucleatum, недавнее исследование на человеке показало, что более высокое содержание F. nucleatum коррелировало с меньшим количеством CD3 + T-клеток при биопсии тканей при КРР, что предполагает возможный иммуносупрессивный эффект, связанный с прогрессированием КРР [32]. Таким образом, разумно предположить, что F. nucleatum может играть важную роль в инициации / прогрессировании КРР.
Следует отметить, что некоторые другие патогенные бактерии, которые в микробиоте толстой кишки содержатся в относительно небольшом количестве, могут проявлять проонкогенную активность в развитии КРР благодаря действию уникальных факторов вирулентности [33]. В качестве примера было представлено предположение о том, что энтеротоксигенный Bacteroides fragilis (ETBF) является ключевым патогеном в инициации КРР; хотя ETBF обычно составляет небольшую часть (от 1 до 2%) фекального бактериального сообщества человека, он вызывает значительные проканцерогенные эффекты, связанные с его способностью к распространению [20,21]. Токсин B. fragilis, токсин металлопротеазы, секретируемый ETBF, может приводить к рекрутированию Т-хелперных клеток 17-го типа (Тх17), которые, в свою очередь, вызывают быстрые и сильные воспалительные реакции, характеризующиеся продукцией генотоксических кислородных радикалов, одновременно подавляя Т-опосредованный опухолевый иммунный надзор посредством селективной активации сигнального преобразователя активатора транскрипции 3 (STAT3)-зависимого пути в толстой кишке человека [20, 21, 34, 35]. Таким образом, возможно, что некоторые бактерии, проявляя агрессивное поведение подобно ETBF, могут быть основной причиной развития КРР. В этом контексте следует упомянуть гипотезу «альфа-ошибки». Эта гипотеза, постулированная Sears и Pardoll [21], вместе с аналогичной гипотезой о «ключевом патогене», предложенной Hajishengallis и коллегами [20], утверждают, что «альфа-ошибка», или «ключевой патоген», такие как ETBF не только вызывает прямую генотоксичность в эпителиальных клетках кишечника, но также вызывает ремоделирование в составе микробиоты толстой кишки. Превосходя антионкогенные симбионты, такие как лактобациллы и бифидобактерии, вызывается проонкогенный иммунный ответ Тх17 (рис. 1). В этом контексте можно считать, что конкретные «альфа-ошибки», или «ключевые патогены» являются основной причиной канцерогенеза КРР, мало чем отличаясь от роли H. pylori в канцерогенезе опухолевых процессов в желудке.
Интересно, что эти ключевые патогены потенциально исчезают во время онкогенной трансформации нормального эпителия в опухолевую ткань во время прогрессирования КРР, потому что они опережают оппортунистические бактерии, которые лучше адаптированы к опухолевой микросреде [7, 9, 22, 33]. Tjalsma и соавт. [22] назвали этот процесс моделью «водитель-пассажир» (рис. 1). В этой модели местные патогенные бактерии, колонизирующие толстую кишку, продуцируют генотоксины, называемые «бактериальными водителями». Примерами являются токсин B. fragilis (BFT, также называемый фрагилисином), колибактин и цитолетальный разрыхляющий токсин (CDT). Изменения в микросреде опухоли, вызванные патогеном-водителем, по-видимому, запускают провоспалительные реакции, которые способны индуцировать последующие изменения в многочисленных внутренних патогенах (ETBF или других патогенах-водителях) в микробном сообществе толстой кишки. Это, в свою очередь, может привести к увеличению числа условно-патогенных микроорганизмов (патогенов-пассажиров), таких как Fusobacterium spp. и Streptococcus spp., которые постепенно вытесняют патогенов-водителей во всем микробном сообществе, что ведет к дальнейшему прогрессированию КРР [7, 9, 22, 33]. Например, патоген-водитель ETBF может сначала колонизировать слизистую оболочку кишечника и впоследствии вызывать Тh17-зависимый иммунный ответ. Это может привести к увеличению пролиферации в кишечном эпителии - например, за счет активации протоонкогена K-Ras (KRAS) и протоонкогена B-Raf (BRAF) или посредством мутаций с потерей функций в генах-супрессорах опухолей, как при аденоматозном полипозе кишечника (APC). Соответственно, измененная микросреда может затем позволить «патогенам-пассажирам», таким как Fusobacterium spp. или Streptococcus spp., превосходя ETBF, колонизировать слизистую, способствуя прогрессированию КРР [22, 36]. В конце концов, состав микробиоты слизистой оболочки человека и мыши может быть резко изменен [22, 33, 34]. В поддержку этих данных в нескольких исследованиях сообщается о пространственном изменении микробного разнообразия между микробиотой просвета кишки и ее слизистой оболочки как в нормальной, так и в воспаленной кишке человека и мыши [37, 38]. Пространственная неоднородность кишечной микробиоты в просвете кишки и ее слизистой оболочке может способствовать изменениям в микробном разнообразии и численности микроорганизмов в воспаленной кишке, которые затем могут привести к развитию КРР.
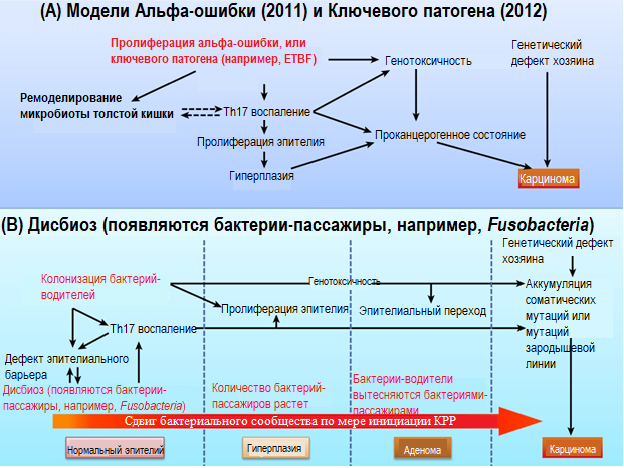 Рисунок 1. Схематическое изображение выдающихся гипотез бактериального канцерогенеза толстой кишки. (A) Проканцерогенное состояние кишечных эпителиальных клеток обусловлено так называемой «альфа-ошибкой», или «ключевым патогеном», таким как энтеротоксигенный Bacteroides fragilis (ETBF), и связано не только с продукцией генотоксинов, которые непосредственно вызывают повреждение ДНК, воспалительные реакции, зависящие от Т-хелперных клеток типа 17 (Tх17), и пролиферацию эпителия (среди прочих характеристик). Гипотеза утверждает, что ремоделирование состава микробиоты слизистой оболочки является основной движущей силой, которая усугубляет и поддерживает воспаление и пролиферацию эпителия. В совокупности все эти факторы способствуют накоплению генетических мутаций и гиперплазии эпителия. Гиперплазия эпителия совместно с генетическими факторами хозяина, связанными с восприимчивостью к колоректальному раку (КРР) и другими проонкогенными детерминантами, могут совместно инициировать рак толстой кишки.
Рисунок 1. Схематическое изображение выдающихся гипотез бактериального канцерогенеза толстой кишки. (A) Проканцерогенное состояние кишечных эпителиальных клеток обусловлено так называемой «альфа-ошибкой», или «ключевым патогеном», таким как энтеротоксигенный Bacteroides fragilis (ETBF), и связано не только с продукцией генотоксинов, которые непосредственно вызывают повреждение ДНК, воспалительные реакции, зависящие от Т-хелперных клеток типа 17 (Tх17), и пролиферацию эпителия (среди прочих характеристик). Гипотеза утверждает, что ремоделирование состава микробиоты слизистой оболочки является основной движущей силой, которая усугубляет и поддерживает воспаление и пролиферацию эпителия. В совокупности все эти факторы способствуют накоплению генетических мутаций и гиперплазии эпителия. Гиперплазия эпителия совместно с генетическими факторами хозяина, связанными с восприимчивостью к колоректальному раку (КРР) и другими проонкогенными детерминантами, могут совместно инициировать рак толстой кишки.
(B) Гипотеза «бактериальный водитель-пассажир» говорит о том, что колонизация толстой кишки предполагаемыми бактериями-водителями (например, ETBF), которые обладают инвазивными характеристиками, может инициировать развитие КРР. Бактериальный фактор также вызывает дефект эпителиального барьера, вызывая последующую колонизацию условно патогенных (пассажирских) патогенов в слизистой оболочке толстой кишки и приводя к микробному дисбиозу кишечника. Th17-зависимое воспаление, вызываемое водителем-патогеном, также может приводить к изменениям в микробном окружении опухоли, что может способствовать селективному стрессу и последующим изменениям в сообществе микробов толстой кишки. В этой модели водители-патогены вытесняются пассажирами-патогенами, что, в свою очередь, приводит к дальнейшему прогрессированию КРР.
Организация биопленки может быть необходимой для инициирования бактериями КРР
Экологические ограничения в кишечнике человека способствуют более высокому уровню пространственной организации мультиорганизменных структур в микробных сообществах слизистой оболочки, из которых наиболее известным является формирование биопленки [11, 13, 39]. Такие биопленки вызывают хронические бактериальные инфекции и не всегда легко поддаются эрадикации. Биопленки, по-видимому, являются важным этиологическим фактором некоторых инфекционных заболеваний человека, особенно эндокардита и кистозного легочного фиброза [40, 41]. Что касается первого, адгезия Streptococcus spp. к белкам внеклеточного матрикса эндотелиальных клеток человека и последующее образование биопленки были ассоциированы с эндокардитом [41]. Недавно обнаружилась связь биопленок с инициацией и развитием КРР - особенно в правой половине ободочной кишки человека (здесь определяется как проксимальный отдел толстой ободочной кишки по отношению к печеночному изгибу) [11]. Биопленки гораздо более распространены в образцах тканей толстой кишки пациентов с КРР, чем в здоровых контрольных образцах [11]. Появляется вероятность того, что биопленки содержат различные виды бактерий, а не только изолированный вид, и могут привести к усилению воспалительных реакций и продукции генотоксичных соединений, полученных из бактерий. Соответственно, Fusobacteria-доминантные полимикробные биопленки, как было показано, в изобилии присутствуют в образцах опухолей, полученных у пациентов с колоректальнымыми аденомами и раком, но отсутствуют в окружающей ткани без опухоли [11]. Биопленки бактерий-водителей могут создавать новые экологические ниши в развитии КРР для бактерий-пассажиров. Согласно модели последовательности аденома-карцинома, предложенной Fearon и Vogelstein [42], микробная биопленка может рассматриваться как независимый «водитель» на ранней стадии канцерогенеза КРР, еще до злокачественной трансформации из аденомы в карциному (Вставка 1). Были предложены к рассмотрению различные процессы, опосредующие действие биопленок при инициации КРР, и они включают в себя присутствие пониженных уровней E-кадгерина в криптах кишечника человека, повышенную проницаемость кишечника, продукцию метаболитов полиаминов и их последующее ацетилирование и повышенную индукцию передачи сигналов ИЛ-6 / STAT3 (рисунок 2) [11, 13]. Таким образом, для стимулирования канцерогенеза КРР микробным патогенам могут потребоваться биопленки.
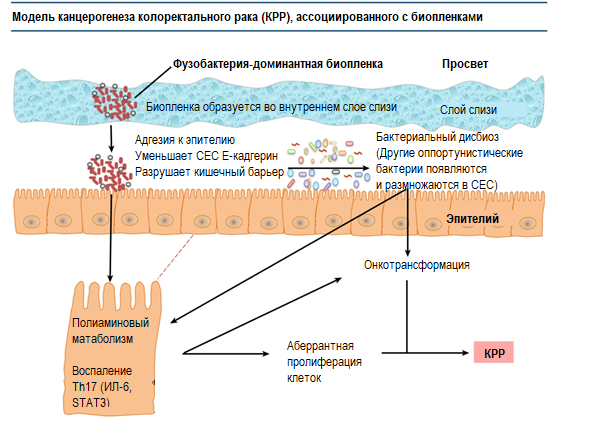 Рисунок 2. Биопленка во внутреннем слое слизистой оболочки толстой кишки приводит к перераспределению E-кадгерина в эпителиальных клетках толстой кишки (CECs), повышенной проницаемости кишечника и потере его барьерной функции, что, в свою очередь, усиливает дисбактериоз кишечника. Дисбиоз может способствовать усилению пролиферации других условно патогенных инвазивных бактерий (то есть пассажиров). Проонкогенные функции бактериальной биопленки и впоследствии бактерий-пассажиров в сочетании с метаболическими изменениями бактериальных полиаминов и воспалением, опосредованным Т-хелпером 17-го типа (Th17), приводят к пролиферации, трансформации и аберрантному росту опухоли.
Рисунок 2. Биопленка во внутреннем слое слизистой оболочки толстой кишки приводит к перераспределению E-кадгерина в эпителиальных клетках толстой кишки (CECs), повышенной проницаемости кишечника и потере его барьерной функции, что, в свою очередь, усиливает дисбактериоз кишечника. Дисбиоз может способствовать усилению пролиферации других условно патогенных инвазивных бактерий (то есть пассажиров). Проонкогенные функции бактериальной биопленки и впоследствии бактерий-пассажиров в сочетании с метаболическими изменениями бактериальных полиаминов и воспалением, опосредованным Т-хелпером 17-го типа (Th17), приводят к пролиферации, трансформации и аберрантному росту опухоли.
Вставка 1. Биопленочный бактериальный туморогенез в толстой и прямой кишке
Инвазивные полимикробные биопленки, по-видимому, важны для ассоциированного с бактериями онкогенеза (рисунок 2) [11]. При КРР, ассоциированном с биопленками, первоначально инвазивные бактерии, такие как Fusobacteria, могут образовывать биопленки, которые напрямую проникают в эпителий кишечника. Эта инвазия биопленки может привести к повышенной проницаемости кишечного эпителия, усилению бактериального дисбиоза, индуцированным воспалительным реакциям и изменениям в метаболоме хозяина/бактерий. В совокупности эти проонкогенные события могут обеспечить генотоксическую и КРР-пермиссивную микросреду, в то время как одновременно могут быть открыты местные экологические ниши, которые позволяют колонизироваться другими микроорганизмами [11, 13]. Таким образом, первоначальный биопленкообразующий организм можно считать водителем (или «альфа-ошибкой») в колоректальном канцерогенезе. Новые организмы, эксплуатирующие созданные экологические ниши, могут усугубить онкогенный процесс благодаря своим специфическим взаимодействиям с хозяином.
Для стимуляции развития КРР биопленкам требуются инвазивные и коагрегационные свойства
Бактериальные биопленки сами по себе не являются канцерогенными, а действуют только в отношении специфических инвазивных бактерий, в особенности фузобактерий [11]. Соответственно, с помощью электронной микроскопии, биопленки были обнаружены в неопухолевой ткани кишки крысы, павиана и человека [43]. Одно исследование также показало, что биопленки могут быть обнаружены в толстой кишке здоровых мышей, и образцы биопленок были получены при проведении колоноскопии у здоровых людей [38]. Кроме того, образцы биопсиийных материалов, полученных при колоноскопии у здоровых людей показали, что тонкие биопленки в слизистой оболочке состоят из относительно безвредных бактерий, в частности, Bacteroidetes, Lachnospiraceae и Enterobacteriaceae в правых отделах толстой ободочной кишки, и Bacteroidetes и Lachnospiraceae (но без Fusobacterium) - в левых отделах ободочной кишки [11]. Большинство, если не все, бактериальные сообщества, обнаруженные в нормальной слизистой оболочке во время этого исследования, являются видами-комменсалами, лишенными инвазивной способности. Таким образом, инвазивный потенциал биопленкообразующих бактерий может иметь отношение к патогенезу КРР. В поддержку этой гипотезы, хотя Fusobacterium spp. и является относительно распространенным и безвредным оппортунистическим патогеном, формирующим биопленки в полости рта, в кишечнике такие биопленки могут провоцировать сильное воспаление [44, 45]. Кроме того, коагрегация F. nucleatum способствует колонизации других видов бактерий в биопленке [46], что позволяет предположить, что образование биопленок действительно может обеспечить новые экологические ниши, таким образом, F. nucleatum может выступать в качестве сильного агента в процессе формирования биопленки. Например, исследование биопленочных культур in vitro показали, что эта бактерия обеспечивает нишу для адгезии и роста Tannerella forsythia, потому что F. nucleatum создает благоприятную среду для облигатных анаэробов. Следовательно, F. nucleatum может привлекать и другие виды бактерий в биопленки [47].
Некоторые виды Campylobacter, такие как C. concisus, C. rectus и C. curvus, являются безвредными колонизаторами полости рта человека, но в то же время в значительной степени ассоциированы с аденокарциномой пищевода и толстой кишки [48]. Некоторые оральные штаммы C. concisus, по-видимому, продуцируют zonula occludens токсин (ZOT), чтобы индуцировать ремоделирование цитоскелета и разрушать плотные соединения эпителиальных клеток кишечника, способствуя транслокации бактерий и инициации воспаления [49]. Campylobacter spp. также способны образовывать биопленку [48, 50]. Например, Campylobacter spp., особенно C. showae, локализуются совместно с видами Fusobacterium и Leptotrichia [50] могут повышать риск возникновения воспалительных заболеваний кишечника (ВЗК) [51]. Было обнаружено, что Leptotrichia spp. значительно чаще встречаются в желудке людей из групп населения с высоким риском развития рака желудка, по сравнению с людьми из групп низкого риска. Предположительно, Leptotrichia spp. также может вызывать рак кишечника [52]. Таким образом, полимикробная ассоциация грамотрицательных анаэробных бактерий, включая Fusobacterium, Campylobacter и Leptotrichia, по-видимому, в значительной степени связана с развитием КРР [50]. Кроме того, существует связь между Streptococcus gallolyticus (ранее известный как Streptococcus bovis) и КРР. Эта бактерия была обнаружена в 20–50% образцов опухоли толстой кишки человека, но менее, чем в 5% образцов, взятых у здоровых людей [12]. Недавние исследования показали, что Streptococcus spp. обладает потенциалом адгезии и способностью образовывать биопленки [41, 53–55]. В совокупности эти наблюдения предполагают, что бактерии, обладающие свойствами инвазии и коагрегации, могут быть необходимым условием для формирования опухолевых биопленок.
Биопленки улучшают взаимодействие между хозяином и микробом при КРР
Бактериальные биопленки могут способствовать увеличению проницаемости кишечника и усилению бактериально-индуцированной потери барьерной функции слизистой, что, в свою очередь, является одним из наиболее важных ранних патофизиологических изменений в колоректальном канцерогенезе [56]. Существует две линии доказательств, подтверждающих концепцию потери барьера за счет биопленок. Во-первых, бактериальная инвазия присутствует во всех колоректальных опухолях человека, при которых обнаружены биопленки, включая КРР и аденомы, но инвазивные признаки отсутствуют в опухолях толстой кишки при отсутствии биопленок [11]. Во-вторых, изображения с помощью сканирующего электронного микроскопа (SEM) и флуоресцентная гибридизация in situ (FISH) показали, что плотные полибактериальные биопленки могут быть обнаружены во всех опухолях правых отделов толстой кишки человека, причем бактериальные сообщества прикрепляются непосредственно к поверхности эпителиальной клетки кишечника, а при опухолях левых отделов толстой кишки биопленки были обнаружены в малом количестве [11]. У пациентов с правосторонним КРР обычно наблюдаются более неблагоприятные клинические исходы, чем у пациентов с левосторонним КРР, что может быть связано разным количеством биопленок справа и слева. Бланодаря биопленке бактерии распространяются в непосредственной близости от кишечного эпителиального барьера, что является необходимым условием для бактериальной инвазии и запуска последующих воспалительных реакций [11, 36, 57]. Потеря кишечного барьера также, по-видимому, усугубляет бактериальный дисбиоз, потому что его неспособность функционировать может способствовать микробной адгезии к эпителиальным клеткам; увеличение проникновения бактериальных продуктов в эпителиальные клетки может затем инициировать создание среды, способствующей образованию опухолей, например, активируя иммунные ответы Th17 и способствуя инициации КРР [11, 36].
Формирование биопленки и усиленная бактериально-опосредованная генотоксичность при КРР
Из возможных механизмов, с помощью которых бактериальные биопленки могут способствовать развитию онкологических заболеваний, генотоксический стресс, вызванный бактериальными токсинами, по-видимому, можно считать одним из основных. Например, различные бактерии продуцируют различные токсины, из которых BFT и CDT способствуют генотоксичности и инициации КРР у человека [58–63]. Действительно, BFT (генерируется из ETBF) является генотоксином, который косвенно вызывает повреждение ДНК [34, 60, 64]. Например, сообщалось, что BFT в линиях эпителиальных клеток толстой кишки HT29 / C1 и T84 in vitro вызывает активацию сперминоксидазы (SMO), что приводит к индуцированной продукции активных форм кислорода (АФК) [60]. Было высказано предположение, что повышенная продукция АФК активирует воспаление NLRP3 (нуклеотидсвязывающий домен олигомеризации (NOD) - подобный рецептор, содержащий пириновый домен 3), важный активатор врожденных иммунных ответов, который может в дальнейшем вызывать повреждение ДНК [65].
Предполагается, что BFT расщепляет молекулу межклеточной адгезии E-кадгерин в эпителиальных клетках толстой кишки человека (например, HT29 / C1), тем самым нарушая барьерную функцию кишечника [66, 67]. Ухудшение кишечного барьера может привести к усиленной «утечке» микробных продуктов, которые могут способствовать предраковым поражениям толстой кишки (аденома) [36]. Затем, как было показано на мышах CPC-APC, это может привести к воспалительному ответу, связанному с ИЛ-23 / ИЛ-17, вызвать повреждение ДНК и в конечном итоге привести к образованию опухоли [36]. Интересно отметить, что биопленка B. fragilis считается одной из ключевых характеристикой ВЗК, в которой опухолевые эффекты персистирующего воспаления кишечника в настоящее время признаны и хорошо изучены [68]. Действительно, более 60% массы бактериальной биопленки, полученной из образцов пациентов с ВЗК, были отнесены к виду Bacteroides [68]. Кроме того, скорость образования сообществ биопленок in vitro, определенных в образцах пациентов с ВЗК, значительно выше, чем в образцах, взятых у индивидуумов с острым самоограничивающимся колитом или в условиях отсутствия воспаления [68]. Таким образом, разумно предположить, что биопленки, содержащие B. fragilis, особенно эффективны в отношении стимуляции кишечного воспаления и КРР. Мы полагаем, что полимикробные биопленки теоретически могут модулировать микроокружение кишечной опухоли несколькими способами (включая генотоксичность) и способствовать развитию рака толстой кишки.
Биопленки влияют на метаболизм хозяина при КРР
Метаболические взаимодействия между микроорганизмом и хозяином могут прямо или косвенно провоцировать бактериальную прогрессию КРР. Собранные данные дают возможность связывать кишечную микробиоту с регуляцией множественных метаболических путей эндогенных и экзогенных субстратов, таких как вторичный биосинтез желчных кислот, катаболизм полиаминов и активация канцерогенов, которые, в свою очередь, связаны с повышенным риском развития различных видов рака человека, таких как КРР, рак пищевода и рак печени [13, 60, 69–75]. Как хороший пример, дезоксихолевая кислота (DCA, также известная как дезоксихолат), по-видимому, является наиболее важным эндогенным метаболитом, связанным с канцерогенезом КРР у мышей ApcMin / + , также найденная в биоптатах толстой кишки человека [70, 73]. DCA может действовать как природный канцероген, который вызывает онкогенную трансформацию в эпителии пищеварительного тракта, поскольку было показано, что DCA вызывает окислительный стресс, повреждение ДНК и геномную нестабильность в тканях при биопсии пищевода человека, раковых клетках эпителия толстой кишки человека и в мышиных моделях [70, 74, 76]. Кроме того, DCA способствует пролиферации опухолевых клеток и ингибирует апоптоз, активируя передачу сигналов Wnt в мышиных моделях ApcMin / + [73]. Поскольку биопленки, по-видимому, могут обеспечивать высокоэффективный интерфейс для деконъюгации и дегидроксилирования желчных кислот, клетки эпителия, покрытые биопленкой, могут подвергаться воздействию очень высоких концентраций вторичных желчных кислот. Кроме того, такие биопленки также могут быть источниками сероводорода (H2S) и нитрозамина. Было установлено, что эти соединения являются генотоксичными и канцерогенными в моделях крыс и мышей, а также в клеточных линиях рака толстой кишки человека (HT29, HCT116 и SW480), которые вызывают повреждение ДНК и нестабильность генома [77–80]. Таким образом, мы предполагаем, что метаболизм компонентов биопленки, вероятно, будет способствовать канцерогенному потенциалу подлежащего эпителия.
Когда сравниваются неадгезирующиеся и биопленочные бактерии, неадгезирующиеся бактериальные сообщества продуцируют более высокие уровни бутирата, что указывает на то, что различные бактериальные сообщества, демонстрирующие организацию более высокого порядка, могут демонстрировать извращенную продукцию жирных кислот с короткой цепью (SCFA), таких как бутират [81]. Fusobacterium-доминантная биопленка может снижать продукцию SCFA и способствовать развитию онкогенеза КРР. Однако микроб-ассоциированные SCFA, включая бутират, могут также способствовать гиперпролиферации и повышать чувствительность эпителиальных клеток толстой кишки к трансформации, по крайней мере, у мышей ApcMin / + с нарушением репарации (MMR) [82]. Фузобактерия является основным источником бутирата в кишечнике. Интересно, что Fusobacterium не были обнаружены в этой модели мыши [82]. Знание роли SCFA в поддержании стабильности кишечного эпителия или индукции КРР остается ограниченным, но измененная продукция этих метаболитов биопленками, безусловно, требует дальнейшего изучения.
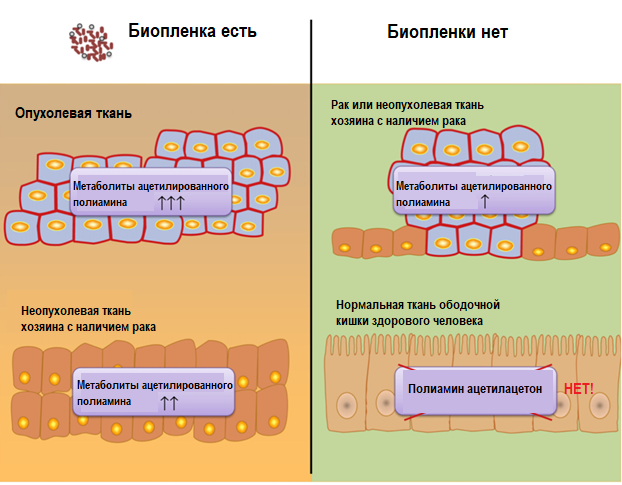 Рисунок 3. Роль ацетилированных полиаминовых метаболитов в развитии колоректального рака (КРР). Схематическое представление различных уровней метаболитов ацетилированных полиаминов у (A) пациентов с наличием биопленок при колоректальном раке (КРР) и (B) пациентов с отсутствием биопленок при КРР или у здоровых людей. Повышенные уровни ацетилированных полиаминов в опухолевых тканях у пациентов, особенно случае наличия тканей КРР, покрытых биопленкой, свидетельствуют о положительной корреляции между патогенезом КРР и наличием биопленок. Метаболиты ацетилированного полиамина не были обнаружены в нормальной ткани толстой кишки (без биопленок) у здоровых людей, что свидетельствует о важной роли биопленок в катаболизме полиаминов. Таким образом, бактериальная биопленка может вносить значительный вклад в повышенное ацетилирование полиамина, которое связано с колоректальным раком.
Рисунок 3. Роль ацетилированных полиаминовых метаболитов в развитии колоректального рака (КРР). Схематическое представление различных уровней метаболитов ацетилированных полиаминов у (A) пациентов с наличием биопленок при колоректальном раке (КРР) и (B) пациентов с отсутствием биопленок при КРР или у здоровых людей. Повышенные уровни ацетилированных полиаминов в опухолевых тканях у пациентов, особенно случае наличия тканей КРР, покрытых биопленкой, свидетельствуют о положительной корреляции между патогенезом КРР и наличием биопленок. Метаболиты ацетилированного полиамина не были обнаружены в нормальной ткани толстой кишки (без биопленок) у здоровых людей, что свидетельствует о важной роли биопленок в катаболизме полиаминов. Таким образом, бактериальная биопленка может вносить значительный вклад в повышенное ацетилирование полиамина, которое связано с колоректальным раком.
Появляются новые данные, свидетельствующие о том, что бактериальные биопленки могут вносить вклад в развитие КРР человека посредством синтеза и ацетилирования полиаминов (рис. 3) [13]. Мультивидовые биопленки экспрессируют бактериальную спермидин / спермин N1-ацетилтрансферазу (SSAT), которая необходима для ацетилирования полиаминов [13]. Важность этого наблюдения подчеркивается данными, показывающими, что экспрессия SSAT у человека не играет значительной роли в формировании опухоли, и, таким образом, бактериальная экспрессия SSAT может иметь значение в этом контексте [13]. Действительно, ацетилированные полиамины существенно повышены как при раке толстой кишки, так и в нормальных тканях при наличии биопленки по сравнению с тканью ободочной кишки, лишенной биопленки [13], что свидетельствует о том, что биопленка усиливает катаболизм и ацетилирование полиаминов, вызывая, в свою очередь, нежелательную пролиферацию и опухолевый рост [60, 83–85]. Кроме того, повышенные уровни метаболитов ацетилированных полиаминов, включая N1-ацетилспермид, N1-ацетилспермин и особенно N1-N12-диацетилспермин, наблюдаются в ткани КРР человека по сравнению с сопоставимыми неопухолевыми тканями тех же пациентов [13]. В соответствии с этим, было обнаружено, что метаболиты полиаминов на границе слизистой оболочки образцов ткани рака толстой кишки (где начинается биопленка) испускают более мощные сигналы, обнаруженные с помощью масс-спектрометрии с визуализацией наноструктуры (NIMS), относительно центра гнезда опухолевых клеток [13]. Этот результат также предполагает, что биопленка может быть наиболее важным источником ацетилированного полиамина [13]. Кроме того, целевой метаболический анализ показал, что в биоптатах толстой кишки здоровых людей без наличия биопленок не было метаболитов ацетилированного полиамина [13]. Эти данные также подтверждают гипотезу о том, что наличие полимикробной биопленки может быть предположительно связано с ростом опухоли в толстой кишке посредством механизма, включающего повышенные уровни метаболитов ацетилированного полиамина.
Полимикробная биопленка как триггер проканцерогенных воспалительных реакций
Вклад бактериального воспаления в процессы опухолевого роста является общепризнанным [34, 86, 87]. В частности, сигнальная ось ИЛ-23 / ИЛ-17, по-видимому, важна при развитии бактериального воспаления [36, 88]. Было показано, что этот путь способствует накоплению гранулоцитов с антибактериальной активностью, но он также может привести к повреждению ДНК у людей и мышей [22, 36, 87]. Более того, гранулоциты особенно склонны к высвобождению провоспалительных цитокинов, таких как ИЛ-1, ИЛ-6 и ИЛ-21 [22, 36]. В значительном объеме литературы также содержится информация о роли ИЛ-17 в развитии и прогрессировании КРР человека [36, 88, 89]. Соответственно, бактериальные токсины, такие как BFT, избирательно стимулируют ИЛ-23 / ИЛ-17-зависимые провоспалительные реакции, вызывая колит у мышей [20, 21, 34]. Например, блокада рецепторов ИЛ-17 и ИЛ-23 (IL23R) с помощью блокирующих антител ингибирует ETBF-индуцированный колит в мышиной модели ApcMin / +, и только Stat3 активируется после колонизации ETBF [34]. В другом примере истощение микробной флоры кишечника у мышей CPC-APC путем кратковременного лечения (3 недели) антибиотиками широкого спектра действия (добавленными в питьевую воду) значительно снижало экспрессию мРНК ИЛ-17А и уменьшало активацию Stat3 в опухолевых клетках толстой кишки [36]. Кроме того, длительное (3,5 месяца) лечение антибиотиками заметно уменьшило размер опухоли толстой кишки у мышей CPC-APC по сравнению с мышами CPC-APC с дефицитом ИЛ23R, что еще раз свидетельствует о том, что вызывающие опухоль кишечные патогены могут быть способны стимулировать ИЛ-23-зависимую проонкогенную передачу сигналов [36]. Действительно, недавние исследования показали значительную положительную связь между распространенностью внутриопухолевых видов Fusobacterium spp. и уровнем белка некоторых воспалительных цитокинов (таких как TNF- и ИЛ-6) в КРР человека, хотя такой корреляции в слизистой оболочке толстой кишки в норме при контроле не обнаружено, что указывает на то, что канцерогенез, вызванный Fusobacteria, может зависеть от способности биопленки провоцировать воспаление слизистой оболочки [29,30]. Следовательно, индукция ИЛ-23 / ИЛ-17-опосредованных иммунных ответов в кишечном эпителии может быть связана с предполагаемым проонкогенным потенциалом биопленочных бактерий.
Накопленные данные также подтверждают идею о том, что биопленки слизистой увеличивают проонкогенный потенциал микробного дисбиоза, вызывая воспалительные реакции [11, 68, 90]. Например, было обнаружено, что концентрация (средняя плотность) адгезивных к слизистой бактерий (образование биопленки) была значительно выше в биоптатах кишки у пациентов с болезнью Крона (БК) по сравнению с невоспалительными контролями, включая пациентов с синдромом раздраженного кишечника (СРК) и здоровых людей. Почти вся микробиота, обнаруженная в кишечном тракте пациента с ВЗК, была адгезирована к эпителию [68]. Микробиота кишечника контролируется взаимодействием между микробной активностью и иммунитетом хозяина и включает высокоорганизованные пространственные структуры микроорганизмов, связанные со специфическими иммунными реакциями [11, 38, 68]. Например, высоковирулентные виды Enterococcus, которые колонизируют кишечный эпителий ободочной и прямой кишки, образуют биопленку, которая защищает бактерии от реактивного кислорода и способствует детоксикации перекиси водорода у пациентов с ВЗК [91]. И наоборот, микробные биопленки также способствуют специфическим иммунным реакциям, которые, в свою очередь, могут стимулировать развитие рака. Как указывалось ранее, биопленки могут непосредственно запускать активацию провоспалительной передачи сигналов ИЛ-6 / STAT3 в эпителиальных клетках кишечника человека, хорошо известный проонкогенный путь. В подтверждение этому, недавнее исследование показало, что уровни ИЛ-6 и фосфорилированного STAT3 в нисходящем направлении были заметно повышены в образцах биопсии неопухолевой ткани больных КРР с наличием биопленок по сравнению с нормальными слизистыми тканями у пациентов с КРР без наличия биопленок [11]. Кроме того, было обнаружено, что ИЛ-6 обладает высокой экспрессией в слизистой оболочке кишечника, покрытой биопленкой, с активацией STAT3, даже у здоровых людей, что позволяет предположить, что биопленка сама по себе может стимулировать воспалительные сигналы ИЛ-6 / STAT3 [11].
Другой пример относится к роли амилоидных фибрилл в процессе воспаления. Эти структуры являются важным общим компонентом биопленки слизистой оболочки [92, 93] и продуцируются доминантными кишечными бактериальными видами, относящимися к типу Firmicutes, Bacteroidetes и Proteobacteria [94]. Амилоидные фибриллы, такие как curli, обеспечивают соответствующие патоген-ассоциированные молекулярные паттерны (PAMP), которые могут индуцировать передачу сигналов Toll-подобного рецептора (TLR) в иммунных клетках [93–96]. Было показано, что сurli, мощный лиганд TLR2 / TLR1, активирует TLR2-зависимый ответ хозяина на моделях колита у мышей (мыши, предварительно обработанные стрептомицином), способствуя вовлечению ИЛ-17A / ИЛ-22 в воспалительные реакции [93–95]. Путем инкубации мышиных CD4 + Т-клеток с супернатантами из дендритных клеток костного мозга (BMDC), предварительно обработанных curli fibrils in vitro, экспрессия и продуцирование ИЛ-17A и ИЛ-22 могут индуцировать дифференцировку наивных CD4 + T-клеток в клетки Tх17 [94]. Таким образом, в целом разумно предположить, что проонкогенная Tх17-зависимая передача сигналов может стимулироваться бактериальной биопленкой, что приводит к воспалению кишечника, которое при тяжелом течении может представлять собой способ, которым биопленки инициируют развитие неоплазии толстой кишки.
Нерешенные вопросы
Каковы точные механизмы канцерогенеза, опосредованного биопленкой, и различаются ли они в правых и левых отделах толстой кишки?
Какую точную роль играет биопленка слизистой оболочки в микробных взаимодействиях между микроорганизмами и организмом-хозяином?
Что может управлять формированием биопленки, связанным с инициацией КРР?
Нужны ли конкретные виды бактерий для формирования бактериальной биопленки? Способствуют ли неспецифические микробы образованию биопленки, инициирующей КРР?
Какие виды бактерий вовлечены в этот процесс? Являются ли они оппортунистическими или патогенными микроорганизмами?
Существуют ли различия в проканцерогенном потенциале различных видов бактерий, формирующих кишечные биопленки?
Можно ли эффективно использовать бактериальную биопленку для выявления раннего рака толстой кишки?
Заключительные замечания
Кишечные бактериальные биопленки и их состав, по-видимому, играют важную роль в запуске и поддержании прогрессирования КРР. Только сейчас становятся более ясными молекулярные механизмы, лежащие в основе перекрестных взаимодействий между бактериальными канцерогенными факторами, бактериальными биопленками и реакциями хозяина при инициации и прогрессировании КРР, и, очевидно, необходимы дальнейшие исследования, чтобы обеспечить понимание механизмов их точного участия в процессе канцерогенеза. Относительная важность этих событий остается неясной, но с появлением программ скрининга КРР для всего населения и связанных с этим возможностей для проведения проспективных исследований представляется вероятным быстрый прогресс в этой области (см. «Нерешенные вопросы» и вставка 2). При рассмотрении различных особенностей пространственной организации микробиоты в тканях правых и левых отделов толстой кишки человека (включая рак и нормальные ткани) следует выставить на рассмотрение важные вопросы о том, имеет ли место образование инвазивной биопленки при раке правой половины толстой кишки у человека [11]. В соответствии с неблагоприятным прогнозом КРР правых отделов кишки [97], мы постулируем, что наличие биопленок в опухолевой ткани при КРР могут приводить к ухудшению клинических результатов по сравнению с опухолями, в которых биопленки отсутствуют, учитывая, что биопленочные сообщества могут вызывать дополнительное серьезное повреждение эпителиальной ткани и воспалительные процессы в кишечнике. Более того, последние появляющиеся данные подтверждают эту гипотезу; показатели ацетилированного спермина могут быть значительно уменьшены в резецированных опухолевых тканях у пациентов с КРР, получавших пероральные антибиотики за 24 часа до операции, по сравнению с образцами опухолевой ткани, покрытыми биопленкой, без предварительного антибактериального лечения [13]. Поэтому мы полагаем, что инициация и прогрессирование КРР являются следствием проонкогенной активности биопленок, состоящих из инвазивных бактерий. Профилактические стратегии, направленные на раннее выявление и ингибирование такого осаждения биопленки, могут оказаться полезными в диагностике и лечении людей с риском развития КРР. Кроме того, среди различных потенциальных терапевтических подходов могут рассматриваться специфические антибиотики, нацеленные на бактериальные биопленки. Однако следует с осторожностью применять такие стратегии при попытке таргетного воздействия на раковые клетки (выборочно или иным образом), поскольку изменение кишечной среды и ее микробиоты может привести к метаболическому дисбалансу и неблагоприятным последствиям для хозяина.
Вставка 2. Уголок врача
В последнее десятилетие ученые с интересом изучали действия изолированного возбудителя, который запускал бы процессы развития КРР и способствовал прогрессированию опухоли, предполагая, что раннее обнаружение конкретного микроорганизма может помочь профилактике и лечению КРР. В последнее время концепция полимикробной синергии вместе с взаимодействиями хозяин-микроб, лежащая в основе бактериального онкогенеза, поставила под сомнение это понятие.
Полибактериальная биопленка (структура бактериальных сообществ высокого порядка) - это не только масса микробных блоков, которая демонстрирует устойчивость к антибиотикам и защитным механизмам организма, но также динамически сложная экосистема, связанная с прогрессированием и тяжестью таких заболеваний как периодонтит, колит и КРР.
Все чаще обнаруживается, что биопленки имеют непосредственное отношение к возникновению различных кишечных заболеваний, особенно к ВЗК и КРР. Многовидовая биопленка потенциально может привести к сильному воспалению кишечника и развитию более агрессивных опухолей толстой кишки.
Для подтверждения важности бактериальной биопленки в развитии КРР у человека необходимы дальнейшие проспективные исследования в группах пациентов с КРР. В случае успеха анализ на наличие инвазивной биопленки может быть использован для улучшения специфичности и чувствительности скрининга населения на КРР. Специально предназначенные для уничтожения инвазивной биопленки новые антибиотики могут рассматриваться как потенциально многообещающие профилактические / терапевтические стратегии при борьбе с КРР.
Глоссарий
Источники
Одним из значимых факторов в инициации и развитии колоректального рака (КРР) является кишечная микробиота. В настоящее время существует распространенное мнение о бактериальном онкогенезе, который заключается в том, что КРР запускается локальной колонизацией слизистой оболочки специфическими патогенными микроорганизмами и что последующие изменения в перитуморозной зоне допускают колонизацию среды оппортунистическими микробами, что еще больше способствует прогрессированию заболевания. Таким образом, скрининг КРР по бактериальной модели «водитель-пассажир» позволяет провести раннюю диагностику КРР или помочь в выборе превентивного вмешательства. Такие попытки в настоящее время аргументируются тем, что для инициирования и развития КРР требуется организация бактериальных сообществ, называемых биопленками. Здесь мы исследуем концепцию, согласно которой полимикробная биопленка способствует проканцерогенной активности.
Тенденции
- Организация бактериальных сообществ в биопленки (пространственные структуры бактериальных видов более высокого порядка) может быть необходимой для инициирования КРР.
- Взаимодействие кишечного эпителия с микробиотой зависит от характера пространственной организации бактериальных сообществ.
- Бактериальные биопленки могут действовать как прямые триггерные факторы, способствующие возникновению колоректального рака.
- Биопленка наделяет оппортунистические бактерии высокоинвазивными свойствами и высоким потенциалом развития опухоли.
- В экспериментальных моделях микробные популяции биопленок могут значительно нарушать барьерную функцию эпителия кишечника, изменять метаболизм полиаминов, влияя на пролиферацию клеток, усиливать провоспалительные / проонкогенные реакции и усугублять дисбиоз кишечника.
- Инвазивная и коагрегационная способность микробиоты может иметь важное значение для стимулированного биопленкой онкогенеза толстой кишки.
Нигде в организме человека микробиом не проявляет свою активностьтак ярко и четко как в желудочно-кишечном тракте (ЖКТ). Здесь обитает около 40 триллионов микробов, представляющих как минимум 1000 видов, подавляющее большинство которых находится в толстой кишке [1]. Таким образом, следует ожидать, что, если микробиом и патофизиология человека взаимосвязаны, это должно быть особенно выражено в толстой кишке. Основная роль микробиома в патофизиологии острых и хронических воспалительных заболеваний толстой кишки действительно хорошо известна [2, 3]. Интересно, что, несмотря на относительно незначительную бактериальную колонизацию желудка, связь между раком желудка и инфекцией Helicobacter pylori не подвергается сомнению. Появляются свидетельства того, что другие микробиоты, колонизирующие желудок, также могут быть задействованы в прогрессировании рака желудка у человека [4, 5]. Причинно-следственная связь между колоректальным раком (КРР) и микробиомом была менее очевидной, однако в последнее время и в этом направлении ученые продвинулись вперед, связав кишечную микробиоту с прогрессированием КРР [6–13]. Такие исследования породили большие надежды на то, что скрининг микробиологических компонентов может обеспечить раннюю диагностику КРР или что заболевание можно потенциально предотвратить с помощью диеты или других вмешательств, которые могут модулировать состав микробиома толстой кишки. Ввиду существенной проблемы КРР в современном обществе такие усилия очень важны [14, 15].
В настоящее время становится ясно, что КРР не зависит от одного конкретного патогенного микроорганизма – на него влияет сложное кишечное бактериальное сообщество. Исследования, сравнивающие анализы кала у пациентов, больных КРР, и относительно здоровых контрольных образцов, продемонстрировали существенные различия в составе их кишечного микробиома [16, 17]. Эти исследования также показывают, что КРР характеризуется микробным дисбиозом [12, 18]. Кроме того, недавние исследования показали, что мыши с дефицитом в иммунном сенсоре Aim2, которые были колонизированы дисбактериальной кишечной микробиотой, стали очень чувствительны к онкогенезу в толстой кишке по сравнению с теми же мышами, колонизированными здоровой микробиотой [19]. Важные вопросы в этой области включают степень, когда эти изменения являются причиной или следствием КРР, в дополнение к выявлению механизмов, опосредующих такие изменения. В настоящее время разрабатываются различные модели бактериального канцерогенеза, что позволяет предположить, как кишечная микробиота, а также взаимодействия микроб-микроб и микроб-хозяин вносят вклад в развитие КРР [20–22]. Тем не менее, механизмы, посредством которых кишечная микробиота взаимодействует с самой собой и человеком-хозяином, вызывая инициацию и прогрессирование КРР, остаются в значительной степени неясными. Становится понятно, что взаимодействия, вызывающие КРР, сильно зависят от природы и пространственной организации мультивидовых бактериальных сообществ в структурах более высокого порядка (так называемых биопленках) [11, 13]. В этой статье мы утверждаем, что полимикробные биопленки способствуют проканцерогенной активности, и что инвазивная биопленка, по-видимому, является необходимой для инициации КРР.
От одного патогенного микроорганизма к полимикробным инфекциям и онкологии
Специфические микроорганизмы сами по себе способны вызывать канцерогенные и другие опухолевые процессы в желудочно-кишечном тракте человека (что очевидно в случае с H. pylori при раке желудка) [23–26]. Кроме того, и другие опухолевые процессы могут быть спровоцированы определенным патогеном, например, рак печени при хроническом вирусном гепатите B или C, рак шейки матки при вирусе папилломы человека, лимфома Беркитта при вирусе Эпштейна-Барр и рак мочевого пузыря, индуцируемый Schistosoma haematobium [20, 21, 27, 28].
Что касается КРР, в двух исследованиях, проведенных в Северной Америке в 2012 году, было обнаружено большое скопление Fusobacterium nucleatum в опухолевой ткани КРР по сравнению с окружающей нормальной тканью [7, 9]. Удалось установить что эта бактерия связана с развитием КРР, о чем свидетельствует ее способность проникать в слизистую оболочку толстой кишки, вызывать местное воспаление и повышенную экспрессию таких цитокинов, как интерлейкин 6 (ИЛ-6), ИЛ-8, ИЛ-12, трансформирующий фактор роста бета (TGF-b) и фактор некроза опухоли (ФНО), и тем самым потенциально усугублять КРР [10, 29, 30]. Бактериальная инфекция F. nucleatum напрямую способствует колоректальному канцерогенезу, о чем свидетельствуют два недавних исследования с использованием мышиной модели ApcMin / + и клеточных линий КРР человека - данные показывают, что инвазия F. nucleatum приводит к рекрутированию инфильтрирующих опухоль иммунных клеток CD11b + (интегрин-субъединица / M, ITGAM) в толстой кишке и созданию онкогенной / провоспалительной микросреды [10, 31]. Более того, данный процесс рекрутирования, по-видимому, зависит от бактериальной адгезии, опосредованной FadA (деградацией адгезиновых жирных кислот A) [10, 31]. Ранее было показано, что FadA связывается с эпителиальным кадгерином (E-cadherin; или кадгерин 1, CDH1), что приводит к активации передачи сигналов b-катенина [31]. Что касается F. nucleatum, недавнее исследование на человеке показало, что более высокое содержание F. nucleatum коррелировало с меньшим количеством CD3 + T-клеток при биопсии тканей при КРР, что предполагает возможный иммуносупрессивный эффект, связанный с прогрессированием КРР [32]. Таким образом, разумно предположить, что F. nucleatum может играть важную роль в инициации / прогрессировании КРР.
Следует отметить, что некоторые другие патогенные бактерии, которые в микробиоте толстой кишки содержатся в относительно небольшом количестве, могут проявлять проонкогенную активность в развитии КРР благодаря действию уникальных факторов вирулентности [33]. В качестве примера было представлено предположение о том, что энтеротоксигенный Bacteroides fragilis (ETBF) является ключевым патогеном в инициации КРР; хотя ETBF обычно составляет небольшую часть (от 1 до 2%) фекального бактериального сообщества человека, он вызывает значительные проканцерогенные эффекты, связанные с его способностью к распространению [20,21]. Токсин B. fragilis, токсин металлопротеазы, секретируемый ETBF, может приводить к рекрутированию Т-хелперных клеток 17-го типа (Тх17), которые, в свою очередь, вызывают быстрые и сильные воспалительные реакции, характеризующиеся продукцией генотоксических кислородных радикалов, одновременно подавляя Т-опосредованный опухолевый иммунный надзор посредством селективной активации сигнального преобразователя активатора транскрипции 3 (STAT3)-зависимого пути в толстой кишке человека [20, 21, 34, 35]. Таким образом, возможно, что некоторые бактерии, проявляя агрессивное поведение подобно ETBF, могут быть основной причиной развития КРР. В этом контексте следует упомянуть гипотезу «альфа-ошибки». Эта гипотеза, постулированная Sears и Pardoll [21], вместе с аналогичной гипотезой о «ключевом патогене», предложенной Hajishengallis и коллегами [20], утверждают, что «альфа-ошибка», или «ключевой патоген», такие как ETBF не только вызывает прямую генотоксичность в эпителиальных клетках кишечника, но также вызывает ремоделирование в составе микробиоты толстой кишки. Превосходя антионкогенные симбионты, такие как лактобациллы и бифидобактерии, вызывается проонкогенный иммунный ответ Тх17 (рис. 1). В этом контексте можно считать, что конкретные «альфа-ошибки», или «ключевые патогены» являются основной причиной канцерогенеза КРР, мало чем отличаясь от роли H. pylori в канцерогенезе опухолевых процессов в желудке.
Интересно, что эти ключевые патогены потенциально исчезают во время онкогенной трансформации нормального эпителия в опухолевую ткань во время прогрессирования КРР, потому что они опережают оппортунистические бактерии, которые лучше адаптированы к опухолевой микросреде [7, 9, 22, 33]. Tjalsma и соавт. [22] назвали этот процесс моделью «водитель-пассажир» (рис. 1). В этой модели местные патогенные бактерии, колонизирующие толстую кишку, продуцируют генотоксины, называемые «бактериальными водителями». Примерами являются токсин B. fragilis (BFT, также называемый фрагилисином), колибактин и цитолетальный разрыхляющий токсин (CDT). Изменения в микросреде опухоли, вызванные патогеном-водителем, по-видимому, запускают провоспалительные реакции, которые способны индуцировать последующие изменения в многочисленных внутренних патогенах (ETBF или других патогенах-водителях) в микробном сообществе толстой кишки. Это, в свою очередь, может привести к увеличению числа условно-патогенных микроорганизмов (патогенов-пассажиров), таких как Fusobacterium spp. и Streptococcus spp., которые постепенно вытесняют патогенов-водителей во всем микробном сообществе, что ведет к дальнейшему прогрессированию КРР [7, 9, 22, 33]. Например, патоген-водитель ETBF может сначала колонизировать слизистую оболочку кишечника и впоследствии вызывать Тh17-зависимый иммунный ответ. Это может привести к увеличению пролиферации в кишечном эпителии - например, за счет активации протоонкогена K-Ras (KRAS) и протоонкогена B-Raf (BRAF) или посредством мутаций с потерей функций в генах-супрессорах опухолей, как при аденоматозном полипозе кишечника (APC). Соответственно, измененная микросреда может затем позволить «патогенам-пассажирам», таким как Fusobacterium spp. или Streptococcus spp., превосходя ETBF, колонизировать слизистую, способствуя прогрессированию КРР [22, 36]. В конце концов, состав микробиоты слизистой оболочки человека и мыши может быть резко изменен [22, 33, 34]. В поддержку этих данных в нескольких исследованиях сообщается о пространственном изменении микробного разнообразия между микробиотой просвета кишки и ее слизистой оболочки как в нормальной, так и в воспаленной кишке человека и мыши [37, 38]. Пространственная неоднородность кишечной микробиоты в просвете кишки и ее слизистой оболочке может способствовать изменениям в микробном разнообразии и численности микроорганизмов в воспаленной кишке, которые затем могут привести к развитию КРР.
 Рисунок 1. Схематическое изображение выдающихся гипотез бактериального канцерогенеза толстой кишки. (A) Проканцерогенное состояние кишечных эпителиальных клеток обусловлено так называемой «альфа-ошибкой», или «ключевым патогеном», таким как энтеротоксигенный Bacteroides fragilis (ETBF), и связано не только с продукцией генотоксинов, которые непосредственно вызывают повреждение ДНК, воспалительные реакции, зависящие от Т-хелперных клеток типа 17 (Tх17), и пролиферацию эпителия (среди прочих характеристик). Гипотеза утверждает, что ремоделирование состава микробиоты слизистой оболочки является основной движущей силой, которая усугубляет и поддерживает воспаление и пролиферацию эпителия. В совокупности все эти факторы способствуют накоплению генетических мутаций и гиперплазии эпителия. Гиперплазия эпителия совместно с генетическими факторами хозяина, связанными с восприимчивостью к колоректальному раку (КРР) и другими проонкогенными детерминантами, могут совместно инициировать рак толстой кишки.
Рисунок 1. Схематическое изображение выдающихся гипотез бактериального канцерогенеза толстой кишки. (A) Проканцерогенное состояние кишечных эпителиальных клеток обусловлено так называемой «альфа-ошибкой», или «ключевым патогеном», таким как энтеротоксигенный Bacteroides fragilis (ETBF), и связано не только с продукцией генотоксинов, которые непосредственно вызывают повреждение ДНК, воспалительные реакции, зависящие от Т-хелперных клеток типа 17 (Tх17), и пролиферацию эпителия (среди прочих характеристик). Гипотеза утверждает, что ремоделирование состава микробиоты слизистой оболочки является основной движущей силой, которая усугубляет и поддерживает воспаление и пролиферацию эпителия. В совокупности все эти факторы способствуют накоплению генетических мутаций и гиперплазии эпителия. Гиперплазия эпителия совместно с генетическими факторами хозяина, связанными с восприимчивостью к колоректальному раку (КРР) и другими проонкогенными детерминантами, могут совместно инициировать рак толстой кишки.(B) Гипотеза «бактериальный водитель-пассажир» говорит о том, что колонизация толстой кишки предполагаемыми бактериями-водителями (например, ETBF), которые обладают инвазивными характеристиками, может инициировать развитие КРР. Бактериальный фактор также вызывает дефект эпителиального барьера, вызывая последующую колонизацию условно патогенных (пассажирских) патогенов в слизистой оболочке толстой кишки и приводя к микробному дисбиозу кишечника. Th17-зависимое воспаление, вызываемое водителем-патогеном, также может приводить к изменениям в микробном окружении опухоли, что может способствовать селективному стрессу и последующим изменениям в сообществе микробов толстой кишки. В этой модели водители-патогены вытесняются пассажирами-патогенами, что, в свою очередь, приводит к дальнейшему прогрессированию КРР.
Организация биопленки может быть необходимой для инициирования бактериями КРР
Экологические ограничения в кишечнике человека способствуют более высокому уровню пространственной организации мультиорганизменных структур в микробных сообществах слизистой оболочки, из которых наиболее известным является формирование биопленки [11, 13, 39]. Такие биопленки вызывают хронические бактериальные инфекции и не всегда легко поддаются эрадикации. Биопленки, по-видимому, являются важным этиологическим фактором некоторых инфекционных заболеваний человека, особенно эндокардита и кистозного легочного фиброза [40, 41]. Что касается первого, адгезия Streptococcus spp. к белкам внеклеточного матрикса эндотелиальных клеток человека и последующее образование биопленки были ассоциированы с эндокардитом [41]. Недавно обнаружилась связь биопленок с инициацией и развитием КРР - особенно в правой половине ободочной кишки человека (здесь определяется как проксимальный отдел толстой ободочной кишки по отношению к печеночному изгибу) [11]. Биопленки гораздо более распространены в образцах тканей толстой кишки пациентов с КРР, чем в здоровых контрольных образцах [11]. Появляется вероятность того, что биопленки содержат различные виды бактерий, а не только изолированный вид, и могут привести к усилению воспалительных реакций и продукции генотоксичных соединений, полученных из бактерий. Соответственно, Fusobacteria-доминантные полимикробные биопленки, как было показано, в изобилии присутствуют в образцах опухолей, полученных у пациентов с колоректальнымыми аденомами и раком, но отсутствуют в окружающей ткани без опухоли [11]. Биопленки бактерий-водителей могут создавать новые экологические ниши в развитии КРР для бактерий-пассажиров. Согласно модели последовательности аденома-карцинома, предложенной Fearon и Vogelstein [42], микробная биопленка может рассматриваться как независимый «водитель» на ранней стадии канцерогенеза КРР, еще до злокачественной трансформации из аденомы в карциному (Вставка 1). Были предложены к рассмотрению различные процессы, опосредующие действие биопленок при инициации КРР, и они включают в себя присутствие пониженных уровней E-кадгерина в криптах кишечника человека, повышенную проницаемость кишечника, продукцию метаболитов полиаминов и их последующее ацетилирование и повышенную индукцию передачи сигналов ИЛ-6 / STAT3 (рисунок 2) [11, 13]. Таким образом, для стимулирования канцерогенеза КРР микробным патогенам могут потребоваться биопленки.
 Рисунок 2. Биопленка во внутреннем слое слизистой оболочки толстой кишки приводит к перераспределению E-кадгерина в эпителиальных клетках толстой кишки (CECs), повышенной проницаемости кишечника и потере его барьерной функции, что, в свою очередь, усиливает дисбактериоз кишечника. Дисбиоз может способствовать усилению пролиферации других условно патогенных инвазивных бактерий (то есть пассажиров). Проонкогенные функции бактериальной биопленки и впоследствии бактерий-пассажиров в сочетании с метаболическими изменениями бактериальных полиаминов и воспалением, опосредованным Т-хелпером 17-го типа (Th17), приводят к пролиферации, трансформации и аберрантному росту опухоли.
Рисунок 2. Биопленка во внутреннем слое слизистой оболочки толстой кишки приводит к перераспределению E-кадгерина в эпителиальных клетках толстой кишки (CECs), повышенной проницаемости кишечника и потере его барьерной функции, что, в свою очередь, усиливает дисбактериоз кишечника. Дисбиоз может способствовать усилению пролиферации других условно патогенных инвазивных бактерий (то есть пассажиров). Проонкогенные функции бактериальной биопленки и впоследствии бактерий-пассажиров в сочетании с метаболическими изменениями бактериальных полиаминов и воспалением, опосредованным Т-хелпером 17-го типа (Th17), приводят к пролиферации, трансформации и аберрантному росту опухоли.Вставка 1. Биопленочный бактериальный туморогенез в толстой и прямой кишке
Инвазивные полимикробные биопленки, по-видимому, важны для ассоциированного с бактериями онкогенеза (рисунок 2) [11]. При КРР, ассоциированном с биопленками, первоначально инвазивные бактерии, такие как Fusobacteria, могут образовывать биопленки, которые напрямую проникают в эпителий кишечника. Эта инвазия биопленки может привести к повышенной проницаемости кишечного эпителия, усилению бактериального дисбиоза, индуцированным воспалительным реакциям и изменениям в метаболоме хозяина/бактерий. В совокупности эти проонкогенные события могут обеспечить генотоксическую и КРР-пермиссивную микросреду, в то время как одновременно могут быть открыты местные экологические ниши, которые позволяют колонизироваться другими микроорганизмами [11, 13]. Таким образом, первоначальный биопленкообразующий организм можно считать водителем (или «альфа-ошибкой») в колоректальном канцерогенезе. Новые организмы, эксплуатирующие созданные экологические ниши, могут усугубить онкогенный процесс благодаря своим специфическим взаимодействиям с хозяином.
Для стимуляции развития КРР биопленкам требуются инвазивные и коагрегационные свойства
Бактериальные биопленки сами по себе не являются канцерогенными, а действуют только в отношении специфических инвазивных бактерий, в особенности фузобактерий [11]. Соответственно, с помощью электронной микроскопии, биопленки были обнаружены в неопухолевой ткани кишки крысы, павиана и человека [43]. Одно исследование также показало, что биопленки могут быть обнаружены в толстой кишке здоровых мышей, и образцы биопленок были получены при проведении колоноскопии у здоровых людей [38]. Кроме того, образцы биопсиийных материалов, полученных при колоноскопии у здоровых людей показали, что тонкие биопленки в слизистой оболочке состоят из относительно безвредных бактерий, в частности, Bacteroidetes, Lachnospiraceae и Enterobacteriaceae в правых отделах толстой ободочной кишки, и Bacteroidetes и Lachnospiraceae (но без Fusobacterium) - в левых отделах ободочной кишки [11]. Большинство, если не все, бактериальные сообщества, обнаруженные в нормальной слизистой оболочке во время этого исследования, являются видами-комменсалами, лишенными инвазивной способности. Таким образом, инвазивный потенциал биопленкообразующих бактерий может иметь отношение к патогенезу КРР. В поддержку этой гипотезы, хотя Fusobacterium spp. и является относительно распространенным и безвредным оппортунистическим патогеном, формирующим биопленки в полости рта, в кишечнике такие биопленки могут провоцировать сильное воспаление [44, 45]. Кроме того, коагрегация F. nucleatum способствует колонизации других видов бактерий в биопленке [46], что позволяет предположить, что образование биопленок действительно может обеспечить новые экологические ниши, таким образом, F. nucleatum может выступать в качестве сильного агента в процессе формирования биопленки. Например, исследование биопленочных культур in vitro показали, что эта бактерия обеспечивает нишу для адгезии и роста Tannerella forsythia, потому что F. nucleatum создает благоприятную среду для облигатных анаэробов. Следовательно, F. nucleatum может привлекать и другие виды бактерий в биопленки [47].
Некоторые виды Campylobacter, такие как C. concisus, C. rectus и C. curvus, являются безвредными колонизаторами полости рта человека, но в то же время в значительной степени ассоциированы с аденокарциномой пищевода и толстой кишки [48]. Некоторые оральные штаммы C. concisus, по-видимому, продуцируют zonula occludens токсин (ZOT), чтобы индуцировать ремоделирование цитоскелета и разрушать плотные соединения эпителиальных клеток кишечника, способствуя транслокации бактерий и инициации воспаления [49]. Campylobacter spp. также способны образовывать биопленку [48, 50]. Например, Campylobacter spp., особенно C. showae, локализуются совместно с видами Fusobacterium и Leptotrichia [50] могут повышать риск возникновения воспалительных заболеваний кишечника (ВЗК) [51]. Было обнаружено, что Leptotrichia spp. значительно чаще встречаются в желудке людей из групп населения с высоким риском развития рака желудка, по сравнению с людьми из групп низкого риска. Предположительно, Leptotrichia spp. также может вызывать рак кишечника [52]. Таким образом, полимикробная ассоциация грамотрицательных анаэробных бактерий, включая Fusobacterium, Campylobacter и Leptotrichia, по-видимому, в значительной степени связана с развитием КРР [50]. Кроме того, существует связь между Streptococcus gallolyticus (ранее известный как Streptococcus bovis) и КРР. Эта бактерия была обнаружена в 20–50% образцов опухоли толстой кишки человека, но менее, чем в 5% образцов, взятых у здоровых людей [12]. Недавние исследования показали, что Streptococcus spp. обладает потенциалом адгезии и способностью образовывать биопленки [41, 53–55]. В совокупности эти наблюдения предполагают, что бактерии, обладающие свойствами инвазии и коагрегации, могут быть необходимым условием для формирования опухолевых биопленок.
Биопленки улучшают взаимодействие между хозяином и микробом при КРР
Бактериальные биопленки могут способствовать увеличению проницаемости кишечника и усилению бактериально-индуцированной потери барьерной функции слизистой, что, в свою очередь, является одним из наиболее важных ранних патофизиологических изменений в колоректальном канцерогенезе [56]. Существует две линии доказательств, подтверждающих концепцию потери барьера за счет биопленок. Во-первых, бактериальная инвазия присутствует во всех колоректальных опухолях человека, при которых обнаружены биопленки, включая КРР и аденомы, но инвазивные признаки отсутствуют в опухолях толстой кишки при отсутствии биопленок [11]. Во-вторых, изображения с помощью сканирующего электронного микроскопа (SEM) и флуоресцентная гибридизация in situ (FISH) показали, что плотные полибактериальные биопленки могут быть обнаружены во всех опухолях правых отделов толстой кишки человека, причем бактериальные сообщества прикрепляются непосредственно к поверхности эпителиальной клетки кишечника, а при опухолях левых отделов толстой кишки биопленки были обнаружены в малом количестве [11]. У пациентов с правосторонним КРР обычно наблюдаются более неблагоприятные клинические исходы, чем у пациентов с левосторонним КРР, что может быть связано разным количеством биопленок справа и слева. Бланодаря биопленке бактерии распространяются в непосредственной близости от кишечного эпителиального барьера, что является необходимым условием для бактериальной инвазии и запуска последующих воспалительных реакций [11, 36, 57]. Потеря кишечного барьера также, по-видимому, усугубляет бактериальный дисбиоз, потому что его неспособность функционировать может способствовать микробной адгезии к эпителиальным клеткам; увеличение проникновения бактериальных продуктов в эпителиальные клетки может затем инициировать создание среды, способствующей образованию опухолей, например, активируя иммунные ответы Th17 и способствуя инициации КРР [11, 36].
Формирование биопленки и усиленная бактериально-опосредованная генотоксичность при КРР
Из возможных механизмов, с помощью которых бактериальные биопленки могут способствовать развитию онкологических заболеваний, генотоксический стресс, вызванный бактериальными токсинами, по-видимому, можно считать одним из основных. Например, различные бактерии продуцируют различные токсины, из которых BFT и CDT способствуют генотоксичности и инициации КРР у человека [58–63]. Действительно, BFT (генерируется из ETBF) является генотоксином, который косвенно вызывает повреждение ДНК [34, 60, 64]. Например, сообщалось, что BFT в линиях эпителиальных клеток толстой кишки HT29 / C1 и T84 in vitro вызывает активацию сперминоксидазы (SMO), что приводит к индуцированной продукции активных форм кислорода (АФК) [60]. Было высказано предположение, что повышенная продукция АФК активирует воспаление NLRP3 (нуклеотидсвязывающий домен олигомеризации (NOD) - подобный рецептор, содержащий пириновый домен 3), важный активатор врожденных иммунных ответов, который может в дальнейшем вызывать повреждение ДНК [65].
Предполагается, что BFT расщепляет молекулу межклеточной адгезии E-кадгерин в эпителиальных клетках толстой кишки человека (например, HT29 / C1), тем самым нарушая барьерную функцию кишечника [66, 67]. Ухудшение кишечного барьера может привести к усиленной «утечке» микробных продуктов, которые могут способствовать предраковым поражениям толстой кишки (аденома) [36]. Затем, как было показано на мышах CPC-APC, это может привести к воспалительному ответу, связанному с ИЛ-23 / ИЛ-17, вызвать повреждение ДНК и в конечном итоге привести к образованию опухоли [36]. Интересно отметить, что биопленка B. fragilis считается одной из ключевых характеристикой ВЗК, в которой опухолевые эффекты персистирующего воспаления кишечника в настоящее время признаны и хорошо изучены [68]. Действительно, более 60% массы бактериальной биопленки, полученной из образцов пациентов с ВЗК, были отнесены к виду Bacteroides [68]. Кроме того, скорость образования сообществ биопленок in vitro, определенных в образцах пациентов с ВЗК, значительно выше, чем в образцах, взятых у индивидуумов с острым самоограничивающимся колитом или в условиях отсутствия воспаления [68]. Таким образом, разумно предположить, что биопленки, содержащие B. fragilis, особенно эффективны в отношении стимуляции кишечного воспаления и КРР. Мы полагаем, что полимикробные биопленки теоретически могут модулировать микроокружение кишечной опухоли несколькими способами (включая генотоксичность) и способствовать развитию рака толстой кишки.
Биопленки влияют на метаболизм хозяина при КРР
Метаболические взаимодействия между микроорганизмом и хозяином могут прямо или косвенно провоцировать бактериальную прогрессию КРР. Собранные данные дают возможность связывать кишечную микробиоту с регуляцией множественных метаболических путей эндогенных и экзогенных субстратов, таких как вторичный биосинтез желчных кислот, катаболизм полиаминов и активация канцерогенов, которые, в свою очередь, связаны с повышенным риском развития различных видов рака человека, таких как КРР, рак пищевода и рак печени [13, 60, 69–75]. Как хороший пример, дезоксихолевая кислота (DCA, также известная как дезоксихолат), по-видимому, является наиболее важным эндогенным метаболитом, связанным с канцерогенезом КРР у мышей ApcMin / + , также найденная в биоптатах толстой кишки человека [70, 73]. DCA может действовать как природный канцероген, который вызывает онкогенную трансформацию в эпителии пищеварительного тракта, поскольку было показано, что DCA вызывает окислительный стресс, повреждение ДНК и геномную нестабильность в тканях при биопсии пищевода человека, раковых клетках эпителия толстой кишки человека и в мышиных моделях [70, 74, 76]. Кроме того, DCA способствует пролиферации опухолевых клеток и ингибирует апоптоз, активируя передачу сигналов Wnt в мышиных моделях ApcMin / + [73]. Поскольку биопленки, по-видимому, могут обеспечивать высокоэффективный интерфейс для деконъюгации и дегидроксилирования желчных кислот, клетки эпителия, покрытые биопленкой, могут подвергаться воздействию очень высоких концентраций вторичных желчных кислот. Кроме того, такие биопленки также могут быть источниками сероводорода (H2S) и нитрозамина. Было установлено, что эти соединения являются генотоксичными и канцерогенными в моделях крыс и мышей, а также в клеточных линиях рака толстой кишки человека (HT29, HCT116 и SW480), которые вызывают повреждение ДНК и нестабильность генома [77–80]. Таким образом, мы предполагаем, что метаболизм компонентов биопленки, вероятно, будет способствовать канцерогенному потенциалу подлежащего эпителия.
Когда сравниваются неадгезирующиеся и биопленочные бактерии, неадгезирующиеся бактериальные сообщества продуцируют более высокие уровни бутирата, что указывает на то, что различные бактериальные сообщества, демонстрирующие организацию более высокого порядка, могут демонстрировать извращенную продукцию жирных кислот с короткой цепью (SCFA), таких как бутират [81]. Fusobacterium-доминантная биопленка может снижать продукцию SCFA и способствовать развитию онкогенеза КРР. Однако микроб-ассоциированные SCFA, включая бутират, могут также способствовать гиперпролиферации и повышать чувствительность эпителиальных клеток толстой кишки к трансформации, по крайней мере, у мышей ApcMin / + с нарушением репарации (MMR) [82]. Фузобактерия является основным источником бутирата в кишечнике. Интересно, что Fusobacterium не были обнаружены в этой модели мыши [82]. Знание роли SCFA в поддержании стабильности кишечного эпителия или индукции КРР остается ограниченным, но измененная продукция этих метаболитов биопленками, безусловно, требует дальнейшего изучения.
 Рисунок 3. Роль ацетилированных полиаминовых метаболитов в развитии колоректального рака (КРР). Схематическое представление различных уровней метаболитов ацетилированных полиаминов у (A) пациентов с наличием биопленок при колоректальном раке (КРР) и (B) пациентов с отсутствием биопленок при КРР или у здоровых людей. Повышенные уровни ацетилированных полиаминов в опухолевых тканях у пациентов, особенно случае наличия тканей КРР, покрытых биопленкой, свидетельствуют о положительной корреляции между патогенезом КРР и наличием биопленок. Метаболиты ацетилированного полиамина не были обнаружены в нормальной ткани толстой кишки (без биопленок) у здоровых людей, что свидетельствует о важной роли биопленок в катаболизме полиаминов. Таким образом, бактериальная биопленка может вносить значительный вклад в повышенное ацетилирование полиамина, которое связано с колоректальным раком.
Рисунок 3. Роль ацетилированных полиаминовых метаболитов в развитии колоректального рака (КРР). Схематическое представление различных уровней метаболитов ацетилированных полиаминов у (A) пациентов с наличием биопленок при колоректальном раке (КРР) и (B) пациентов с отсутствием биопленок при КРР или у здоровых людей. Повышенные уровни ацетилированных полиаминов в опухолевых тканях у пациентов, особенно случае наличия тканей КРР, покрытых биопленкой, свидетельствуют о положительной корреляции между патогенезом КРР и наличием биопленок. Метаболиты ацетилированного полиамина не были обнаружены в нормальной ткани толстой кишки (без биопленок) у здоровых людей, что свидетельствует о важной роли биопленок в катаболизме полиаминов. Таким образом, бактериальная биопленка может вносить значительный вклад в повышенное ацетилирование полиамина, которое связано с колоректальным раком.Появляются новые данные, свидетельствующие о том, что бактериальные биопленки могут вносить вклад в развитие КРР человека посредством синтеза и ацетилирования полиаминов (рис. 3) [13]. Мультивидовые биопленки экспрессируют бактериальную спермидин / спермин N1-ацетилтрансферазу (SSAT), которая необходима для ацетилирования полиаминов [13]. Важность этого наблюдения подчеркивается данными, показывающими, что экспрессия SSAT у человека не играет значительной роли в формировании опухоли, и, таким образом, бактериальная экспрессия SSAT может иметь значение в этом контексте [13]. Действительно, ацетилированные полиамины существенно повышены как при раке толстой кишки, так и в нормальных тканях при наличии биопленки по сравнению с тканью ободочной кишки, лишенной биопленки [13], что свидетельствует о том, что биопленка усиливает катаболизм и ацетилирование полиаминов, вызывая, в свою очередь, нежелательную пролиферацию и опухолевый рост [60, 83–85]. Кроме того, повышенные уровни метаболитов ацетилированных полиаминов, включая N1-ацетилспермид, N1-ацетилспермин и особенно N1-N12-диацетилспермин, наблюдаются в ткани КРР человека по сравнению с сопоставимыми неопухолевыми тканями тех же пациентов [13]. В соответствии с этим, было обнаружено, что метаболиты полиаминов на границе слизистой оболочки образцов ткани рака толстой кишки (где начинается биопленка) испускают более мощные сигналы, обнаруженные с помощью масс-спектрометрии с визуализацией наноструктуры (NIMS), относительно центра гнезда опухолевых клеток [13]. Этот результат также предполагает, что биопленка может быть наиболее важным источником ацетилированного полиамина [13]. Кроме того, целевой метаболический анализ показал, что в биоптатах толстой кишки здоровых людей без наличия биопленок не было метаболитов ацетилированного полиамина [13]. Эти данные также подтверждают гипотезу о том, что наличие полимикробной биопленки может быть предположительно связано с ростом опухоли в толстой кишке посредством механизма, включающего повышенные уровни метаболитов ацетилированного полиамина.
Полимикробная биопленка как триггер проканцерогенных воспалительных реакций
Вклад бактериального воспаления в процессы опухолевого роста является общепризнанным [34, 86, 87]. В частности, сигнальная ось ИЛ-23 / ИЛ-17, по-видимому, важна при развитии бактериального воспаления [36, 88]. Было показано, что этот путь способствует накоплению гранулоцитов с антибактериальной активностью, но он также может привести к повреждению ДНК у людей и мышей [22, 36, 87]. Более того, гранулоциты особенно склонны к высвобождению провоспалительных цитокинов, таких как ИЛ-1, ИЛ-6 и ИЛ-21 [22, 36]. В значительном объеме литературы также содержится информация о роли ИЛ-17 в развитии и прогрессировании КРР человека [36, 88, 89]. Соответственно, бактериальные токсины, такие как BFT, избирательно стимулируют ИЛ-23 / ИЛ-17-зависимые провоспалительные реакции, вызывая колит у мышей [20, 21, 34]. Например, блокада рецепторов ИЛ-17 и ИЛ-23 (IL23R) с помощью блокирующих антител ингибирует ETBF-индуцированный колит в мышиной модели ApcMin / +, и только Stat3 активируется после колонизации ETBF [34]. В другом примере истощение микробной флоры кишечника у мышей CPC-APC путем кратковременного лечения (3 недели) антибиотиками широкого спектра действия (добавленными в питьевую воду) значительно снижало экспрессию мРНК ИЛ-17А и уменьшало активацию Stat3 в опухолевых клетках толстой кишки [36]. Кроме того, длительное (3,5 месяца) лечение антибиотиками заметно уменьшило размер опухоли толстой кишки у мышей CPC-APC по сравнению с мышами CPC-APC с дефицитом ИЛ23R, что еще раз свидетельствует о том, что вызывающие опухоль кишечные патогены могут быть способны стимулировать ИЛ-23-зависимую проонкогенную передачу сигналов [36]. Действительно, недавние исследования показали значительную положительную связь между распространенностью внутриопухолевых видов Fusobacterium spp. и уровнем белка некоторых воспалительных цитокинов (таких как TNF- и ИЛ-6) в КРР человека, хотя такой корреляции в слизистой оболочке толстой кишки в норме при контроле не обнаружено, что указывает на то, что канцерогенез, вызванный Fusobacteria, может зависеть от способности биопленки провоцировать воспаление слизистой оболочки [29,30]. Следовательно, индукция ИЛ-23 / ИЛ-17-опосредованных иммунных ответов в кишечном эпителии может быть связана с предполагаемым проонкогенным потенциалом биопленочных бактерий.
Накопленные данные также подтверждают идею о том, что биопленки слизистой увеличивают проонкогенный потенциал микробного дисбиоза, вызывая воспалительные реакции [11, 68, 90]. Например, было обнаружено, что концентрация (средняя плотность) адгезивных к слизистой бактерий (образование биопленки) была значительно выше в биоптатах кишки у пациентов с болезнью Крона (БК) по сравнению с невоспалительными контролями, включая пациентов с синдромом раздраженного кишечника (СРК) и здоровых людей. Почти вся микробиота, обнаруженная в кишечном тракте пациента с ВЗК, была адгезирована к эпителию [68]. Микробиота кишечника контролируется взаимодействием между микробной активностью и иммунитетом хозяина и включает высокоорганизованные пространственные структуры микроорганизмов, связанные со специфическими иммунными реакциями [11, 38, 68]. Например, высоковирулентные виды Enterococcus, которые колонизируют кишечный эпителий ободочной и прямой кишки, образуют биопленку, которая защищает бактерии от реактивного кислорода и способствует детоксикации перекиси водорода у пациентов с ВЗК [91]. И наоборот, микробные биопленки также способствуют специфическим иммунным реакциям, которые, в свою очередь, могут стимулировать развитие рака. Как указывалось ранее, биопленки могут непосредственно запускать активацию провоспалительной передачи сигналов ИЛ-6 / STAT3 в эпителиальных клетках кишечника человека, хорошо известный проонкогенный путь. В подтверждение этому, недавнее исследование показало, что уровни ИЛ-6 и фосфорилированного STAT3 в нисходящем направлении были заметно повышены в образцах биопсии неопухолевой ткани больных КРР с наличием биопленок по сравнению с нормальными слизистыми тканями у пациентов с КРР без наличия биопленок [11]. Кроме того, было обнаружено, что ИЛ-6 обладает высокой экспрессией в слизистой оболочке кишечника, покрытой биопленкой, с активацией STAT3, даже у здоровых людей, что позволяет предположить, что биопленка сама по себе может стимулировать воспалительные сигналы ИЛ-6 / STAT3 [11].
Другой пример относится к роли амилоидных фибрилл в процессе воспаления. Эти структуры являются важным общим компонентом биопленки слизистой оболочки [92, 93] и продуцируются доминантными кишечными бактериальными видами, относящимися к типу Firmicutes, Bacteroidetes и Proteobacteria [94]. Амилоидные фибриллы, такие как curli, обеспечивают соответствующие патоген-ассоциированные молекулярные паттерны (PAMP), которые могут индуцировать передачу сигналов Toll-подобного рецептора (TLR) в иммунных клетках [93–96]. Было показано, что сurli, мощный лиганд TLR2 / TLR1, активирует TLR2-зависимый ответ хозяина на моделях колита у мышей (мыши, предварительно обработанные стрептомицином), способствуя вовлечению ИЛ-17A / ИЛ-22 в воспалительные реакции [93–95]. Путем инкубации мышиных CD4 + Т-клеток с супернатантами из дендритных клеток костного мозга (BMDC), предварительно обработанных curli fibrils in vitro, экспрессия и продуцирование ИЛ-17A и ИЛ-22 могут индуцировать дифференцировку наивных CD4 + T-клеток в клетки Tх17 [94]. Таким образом, в целом разумно предположить, что проонкогенная Tх17-зависимая передача сигналов может стимулироваться бактериальной биопленкой, что приводит к воспалению кишечника, которое при тяжелом течении может представлять собой способ, которым биопленки инициируют развитие неоплазии толстой кишки.
Нерешенные вопросы
Каковы точные механизмы канцерогенеза, опосредованного биопленкой, и различаются ли они в правых и левых отделах толстой кишки?
Какую точную роль играет биопленка слизистой оболочки в микробных взаимодействиях между микроорганизмами и организмом-хозяином?
Что может управлять формированием биопленки, связанным с инициацией КРР?
Нужны ли конкретные виды бактерий для формирования бактериальной биопленки? Способствуют ли неспецифические микробы образованию биопленки, инициирующей КРР?
Какие виды бактерий вовлечены в этот процесс? Являются ли они оппортунистическими или патогенными микроорганизмами?
Существуют ли различия в проканцерогенном потенциале различных видов бактерий, формирующих кишечные биопленки?
Можно ли эффективно использовать бактериальную биопленку для выявления раннего рака толстой кишки?
Заключительные замечания
Кишечные бактериальные биопленки и их состав, по-видимому, играют важную роль в запуске и поддержании прогрессирования КРР. Только сейчас становятся более ясными молекулярные механизмы, лежащие в основе перекрестных взаимодействий между бактериальными канцерогенными факторами, бактериальными биопленками и реакциями хозяина при инициации и прогрессировании КРР, и, очевидно, необходимы дальнейшие исследования, чтобы обеспечить понимание механизмов их точного участия в процессе канцерогенеза. Относительная важность этих событий остается неясной, но с появлением программ скрининга КРР для всего населения и связанных с этим возможностей для проведения проспективных исследований представляется вероятным быстрый прогресс в этой области (см. «Нерешенные вопросы» и вставка 2). При рассмотрении различных особенностей пространственной организации микробиоты в тканях правых и левых отделов толстой кишки человека (включая рак и нормальные ткани) следует выставить на рассмотрение важные вопросы о том, имеет ли место образование инвазивной биопленки при раке правой половины толстой кишки у человека [11]. В соответствии с неблагоприятным прогнозом КРР правых отделов кишки [97], мы постулируем, что наличие биопленок в опухолевой ткани при КРР могут приводить к ухудшению клинических результатов по сравнению с опухолями, в которых биопленки отсутствуют, учитывая, что биопленочные сообщества могут вызывать дополнительное серьезное повреждение эпителиальной ткани и воспалительные процессы в кишечнике. Более того, последние появляющиеся данные подтверждают эту гипотезу; показатели ацетилированного спермина могут быть значительно уменьшены в резецированных опухолевых тканях у пациентов с КРР, получавших пероральные антибиотики за 24 часа до операции, по сравнению с образцами опухолевой ткани, покрытыми биопленкой, без предварительного антибактериального лечения [13]. Поэтому мы полагаем, что инициация и прогрессирование КРР являются следствием проонкогенной активности биопленок, состоящих из инвазивных бактерий. Профилактические стратегии, направленные на раннее выявление и ингибирование такого осаждения биопленки, могут оказаться полезными в диагностике и лечении людей с риском развития КРР. Кроме того, среди различных потенциальных терапевтических подходов могут рассматриваться специфические антибиотики, нацеленные на бактериальные биопленки. Однако следует с осторожностью применять такие стратегии при попытке таргетного воздействия на раковые клетки (выборочно или иным образом), поскольку изменение кишечной среды и ее микробиоты может привести к метаболическому дисбалансу и неблагоприятным последствиям для хозяина.
Вставка 2. Уголок врача
В последнее десятилетие ученые с интересом изучали действия изолированного возбудителя, который запускал бы процессы развития КРР и способствовал прогрессированию опухоли, предполагая, что раннее обнаружение конкретного микроорганизма может помочь профилактике и лечению КРР. В последнее время концепция полимикробной синергии вместе с взаимодействиями хозяин-микроб, лежащая в основе бактериального онкогенеза, поставила под сомнение это понятие.
Полибактериальная биопленка (структура бактериальных сообществ высокого порядка) - это не только масса микробных блоков, которая демонстрирует устойчивость к антибиотикам и защитным механизмам организма, но также динамически сложная экосистема, связанная с прогрессированием и тяжестью таких заболеваний как периодонтит, колит и КРР.
Все чаще обнаруживается, что биопленки имеют непосредственное отношение к возникновению различных кишечных заболеваний, особенно к ВЗК и КРР. Многовидовая биопленка потенциально может привести к сильному воспалению кишечника и развитию более агрессивных опухолей толстой кишки.
Для подтверждения важности бактериальной биопленки в развитии КРР у человека необходимы дальнейшие проспективные исследования в группах пациентов с КРР. В случае успеха анализ на наличие инвазивной биопленки может быть использован для улучшения специфичности и чувствительности скрининга населения на КРР. Специально предназначенные для уничтожения инвазивной биопленки новые антибиотики могут рассматриваться как потенциально многообещающие профилактические / терапевтические стратегии при борьбе с КРР.
Глоссарий
Источники
- Sender, R. et al. (2016) Are we really vastly outnumbered? Revisiting the ratio of bacterial to host cells in humans. Cell 164, 337–340.
- Thiagarajah, J.R. et al. (2015) Secretory diarrhoea: mechanisms and emerging therapies. Nat. Rev. Gastroenterol. Hepatol. 12, 446–457.
- DuPont, A.W. and DuPont, H.L. (2011) The intestinal microbiota and chronic disorders of the gut. Nat. Rev. Gastroenterol. Hepatol. 8, 523–531.
- Aviles-Jimenez, F. et al. (2014) Stomach microbiota composition varies between patients with non-atrophic gastritis and patients with intestinal type of gastric cancer. Sci. Rep. 4, 4202.
- Eun, C.S. et al. (2014) Differences in gastric mucosal microbiota profiling in patients with chronic gastritis, intestinal metaplasia, and gastric cancer using pyrosequencing methods. Helicobacter 19, 407–416.
- Machida-Montani, A. et al. (2007) Atrophic gastritis, Helicobacter pylori, and colorectal cancer risk: a case-control study. Helicobacter 12, 328–332.
- Castellarin, M. et al. (2012) Fusobacterium nucleatum infection is prevalent in human colorectal carcinoma. Genome Res. 22, 299–306.
- Arthur, J.C. et al. (2014) Microbial genomic analysis reveals the essential role of inflammation in bacteria-induced colorectal cancer. Nat. Commun. 5, 4724.
- Kostic, A.D. et al. (2012) Genomic analysis identifies association of Fusobacterium with colorectal carcinoma. Genome Res. 22, 292–298.
- Kostic, A.D. et al. (2013) Fusobacterium nucleatum potentiates intestinal tumorigenesis and modulates the tumor-immune microenvironment. Cell Host Microbe 14, 207–215.
- Dejea, C.M. et al. (2014) Microbiota organization is a distinct feature of proximal colorectal cancers. Proc. Natl. Acad. Sci. U. S. A. 111, 18321–18326.
- Gao, Z.G. et al. (2015) Microbiota disbiosis is associated with colorectal cancer. Front. Microbiol. 6, 20.
- Johnson, C.H. et al. (2015) Metabolism links bacterial biofilms and colon carcinogenesis. Cell. Metab. 21, 891–897.
- Siegel, R. et al. (2014) Colorectal cancer statistics, 2014. CA Cancer J. Clin. 64, 104–117
- Torre, L.A. et al. (2015) Global cancer statistics, 2012. CA Cancer J. Clin. 65, 87–108
- Zackular, J.P. et al. (2014) The human gut microbiome as a screening tool for colorectal cancer. Cancer Prev. Res. 7, 1112–1121.
- Baxter, N.T. et al. (2016) Microbiota-based model improves the sensitivity of fecal immunochemical test for detecting colonic lesions. Genome Med. 8, 37.
- Wu, N. et al. (2013) Dysbiosis signature of fecal microbiota in colorectal cancer patients. Microb. Ecol. 66, 462–470.
- Man, S.M. et al. (2015) Critical role for the DNA sensor AIM2 in stem cell proliferation and cancer. Cell 162, 45–58.
- Hajishengallis, G. et al. (2012) The keystone-pathogen hypothesis. Nat. Rev. Microbiol. 10, 717–725.
- Sears, C.L. and Pardoll, D.M. (2011) Perspective: alpha-bugs, their microbial partners, and the link to colon cancer. J. Infect. Dis. 203, 306–311.
- Tjalsma, H. et al. (2012) A bacterial driver-passenger model for colorectal cancer: beyond the usual suspects. Nat. Rev. Microbiol. 10, 575–582.
- Nomura, A. et al. (1991) Helicobacter pylori infection and gastric carcinoma among Japanese Americans in Hawaii. N. Engl. J. Med. 325, 1132–1136.
- Parsonnet, J. et al. (1991) Helicobacter pylori infection and the risk of gastric carcinoma. N. Engl. J. Med. 325, 1127–1131.
- Talley, N.J. et al. (1991) Gastric adenocarcinoma and Helicobacter pylori infection. J. Natl. Cancer Inst. 83, 1734–1739
- Parsonnet, J. et al. (1991) Helicobacter pylori infection in intestinal- and diffuse-type gastric adenocarcinomas. J. Natl. Cancer Inst. 83, 640–643.
- Trends in Molecular Medicine, January 2017, Vol. 23, No. 1. 28. de Martel, C. et al. (2012) Global burden of cancers attributable to infections in 2008: a review and synthetic analysis. Lancet Oncol. 13, 607–615.
- Zeller, G. et al. (2014) Potential of fecal microbiota for early-stage detection of colorectal cancer. Mol. Syst. Biol. 10, 766.
- Saito, T. et al. (2016) Two FOXP3+CD4+ T cell subpopulations distinctly control the prognosis of colorectal cancers. Nat. Med. 22, 679–684.
- McCoy, A.N. et al. (2013) Fusobacterium is associated with colorectal adenomas. PLoS One 8, e53653.
- Rubinstein, M.R. et al. (2013) Fusobacterium nucleatum promotes colorectal carcinogenesis by modulating E-cadherin/ beta-catenin signaling via its FadA adhesin. Cell Host Microbe 14, 195–206.
- Mima, K. et al. (2015) Fusobacterium nucleatum and T cells in colorectal carcinoma. JAMA Oncol. 1, 653–661.
- Marchesi, J.R. et al. (2011) Towards the human colorectal cancer microbiome. PLoS One 6, e20447.
- Wu, S. et al. (2009) A human colonic commensal promotes colon tumorigenesis via activation of T helper type 17 T cell responses. Nat. Med. 15, 1016–1022.
- Geis, A.L. et al. (2015) Regulatory T-cell response to enterotoxigenic Bacteroides fragilis colonization triggers IL17-dependent colon carcinogenesis. Cancer Discov. 5, 1098–1109.
- Grivennikov, S.I. et al. (2012) Adenoma-linked barrier defects and microbial products drive IL-23/IL-17-mediated tumour growth. Nature 491, 254–258.
- Lavelle, A. et al. (2015) Spatial variation of the colonic microbiota in patients with ulcerative colitis and control volunteers. Gut 64, 1553–1561.
- Swidsinski, A. et al. (2005) Spatial organization of bacterial flora in normal and inflamed intestine: a fluorescence in situ hybridization study in mice. World J. Gastroenterol. 11, 1131– 1140.
- Costerton, J.W. et al. (1983) Colonization of particulates, mucous, and intestinal tissue. Prog. Food Nutr. Sci. 7, 91–105.
- Drenkard, E. and Ausubel, F.M. (2002) Pseudomonas biofilm formation and antibiotic resistance are linked to phenotypic variation. Nature 416, 740–743.
- Vollmer, T. et al. (2010) Interactions between endocarditis-derived Streptococcus gallolyticus subsp. gallolyticus isolates and human endothelial cells. BMC Microbiol. 10, 78.
- Fearon, E.R. and Vogelstein, B. (1990) A genetic model for colorectal tumorigenesis. Cell 61, 759–767.
- Palestrant, D. et al. (2004) Microbial biofilms in the gut: visualization by electron microscopy and by acridine orange staining. Ultrastruct. Pathol. 28, 23–27.
- Swidsinski, A. et al. (2011) Acute appendicitis is characterized by local invasion with Fusobacterium nucleatum/necrophorum. Gut 60, 34–40.
- Strauss, J. et al. (2011) Invasive potential of gut mucosa-derived Fusobacterium nucleatum positively correlates with IBD status of the host. Inflamm. Bowel Dis. 17, 1971–1978.
- Bradshaw, D.J. et al. (1998) Role of Fusobacterium nucleatum and coaggregation in anaerobe survival in planktonic and biofilm oral microbial communities during aeration. Infect. Immun. 66, 4729–4732.
- Sharma, A. et al. (2005) Synergy between Tannerella forsythia and Fusobacterium nucleatum in biofilm formation. Oral Microbiol. Immunol. 20, 39–42.
- Kaakoush, N.O. et al. (2015) Is Campylobacter to esophageal adenocarcinoma as Helicobacter is to gastric adenocarcinoma? Trends Microbiol. 23, 455–462.
- Deshpande, N.P. et al. (2016) Campylobacter concisus pathotypes induce distinct global responses in intestinal epithelial cells. Sci. Rep. 6, 34288.
- Warren, R.L. et al. (2013) Co-occurrence of anaerobic bacteria in colorectal carcinomas. Microbiome 1, 16.
- Castaño-Rodríguez, N. et al. (2015) Dual role of Helicobacter and Campylobacter species in IBD: a systematic review and meta- analysis. Gut Published online October 27, 2015.
- Yang, I. et al. (2016) Different gastric microbiota compositions in two human populations with high and low gastric cancer risk in Colombia. Sci. Rep. 6, 18594.
- Sillanpaa, J. et al. (2009) A collagen-binding adhesin, Acb, and ten other putative MSCRAMM and pilus family proteins of Streptococcus gallolyticus subsp gallolyticus (Streptococcus bovis group, biotype I). J. Bacteriol. 191, 6643–6653.
- Sillanpaa, J. et al. (2008) Adherence characteristics of endocarditis-derived Streptococcus gallolyticus ssp gallolyticus (Streptococcus bovis biotype I) isolates to host extracellular matrix proteins. FEMS Microbiol. Lett. 289, 104–109.
- Boleij, A. et al. (2009) Surface-exposed histone-like protein A modulates adherence of Streptococcus gallolyticus to colon adenocarcinoma cells. Infect. Immun. 77, 5519–5527.
- Soler, A.P. et al. (1999) Increased tight junctional permeability is associated with the development of colon cancer. Carcinogenesis 20, 1425–1431.
- Johansson, M.E.V. et al. (2014) Bacteria penetrate the normally impenetrable inner colon mucus layer in both murine colitis models and patients with ulcerative colitis. Gut 63, 281–291
- Nougayrede, J.P. et al. (2006) Escherichia coli induces DNA double-strand breaks in eukaryotic cells. Science 313, 848–851.
- Cuevas-Ramos, G. et al. (2010) Escherichia coli induces DNA damage in vivo and triggers genomic instability in mammalian cells. Proc. Natl. Acad. Sci. U. S. A. 107, 11537–11542.
- Goodwin, A.C. et al. (2011) Polyamine catabolism contributes to enterotoxigenic Bacteroides fragilis-induced colon tumorigenesis. Proc. Natl. Acad. Sci. U. S. A. 108, 15354–15359.
- Buc, E. et al. (2013) High prevalence of mucosa-associated E. coli producing cyclomodulin and genotoxin in colon cancer. PLoS One 8, e56964.
- Guidi, R. et al. (2013) Chronic exposure to the cytolethal distending toxins of Gram-negative bacteria promotes genomic instability and altered DNA damage response. Cell. Microbiol. 15, 98–113.
- Toprak, N.U. et al. (2006) A possible role of Bacteroides fragilis enterotoxin in the aetiology of colorectal cancer. Clin. Microbiol. Infect. 12, 782–786.
- Kim, J.M. et al. (2008) Inhibition of apoptosis in Bacteroides fragilis enterotoxin-stimulated intestinal epithelial cells through the induction of c-IAP-2. Eur. J. Immunol. 38, 2190–2199.
- Abais, J.M. et al. (2015) Redox regulation of NLRP3 inflammasomes: ROS as trigger or effector? Antioxid. Redox Signal. 22, 1111–1129.
- Wu, S. et al. (2003) Bacteroides fragilis enterotoxin induces c- Myc expression and cellular proliferation. Gastroenterology 124, 392–400.
- Wu, S. et al. (2007) Bacteroides fragilis toxin stimulates intestinal epithelial cell shedding and gamma-secretase-dependent E-cadherin cleavage. J. Cell Sci. 120, 1944–1952.
- Swidsinski, A. et al. (2005) Spatial organization and composition of the mucosal flora in patients with inflammatory bowel disease. J. Clin. Microbiol. 43, 3380–3389.
- Gill, S.R. et al. (2006) Metagenomic analysis of the human distal gut microbiome. Science 312, 1355–1359.
- Bernstein, C. et al. (2011) Carcinogenicity of deoxycholate, a secondary bile acid. Arch. Toxicol. 85, 863–871.
- Yoshimoto, S. et al. (2013) Obesity-induced gut microbial metabolite promotes liver cancer through senescence secretome. Nature 499, 97–101.
- Quante, M. et al. (2012) Bile acid and inflammation activate gastric cardia stem cells in a mouse model of Barrett-like metaplasia. Cancer Cell 21, 36–51.
- Cao, H. et al. (2014) The secondary bile acid, deoxycholate accelerates intestinal adenoma-adenocarcinoma sequence in ApcMin/+ mice through enhancing Wnt signaling. Fam. Cancer 13, 563–571.
- Dvorak, K. et al. (2007) Bile acids in combination with low pH induce oxidative stress and oxidative DNA damage: relevance to the pathogenesis of Barrett's oesophagus. Gut 56, 763–771.
- Russell, W.R. et al. (2013) Major phenylpropanoid-derived metabolites in the human gut can arise from microbial fermentation of protein. Mol. Nutr. Food Res. 57, 523–535.
- Majer, F. et al. (2014) New highly toxic bile acids derived from deoxycholic acid, chenodeoxycholic acid and lithocholic acid. Bioorg. Med. Chem. 22, 256–268.
- Cai, W.J. et al. (2010) Hydrogen sulfide induces human colon cancer cell proliferation: role of Akt, ERK and p21. Cell Biol. Int. 34, 565–572.
- Attene-Ramos, M.S. et al. (2006) Evidence that hydrogen sulfide is a genotoxic agent. Mol. Cancer Res. 4, 9–14.
- Ijssennagger, N. et al. (2015) Gut microbiota facilitates dietary heme-induced epithelial hyperproliferation by opening the mucus barrier in colon. Proc. Natl. Acad. Sci. U. S. A. 112, 10038–10043.
- Alam, B.S. et al. (1971) Synthesis of nitrosopiperidine from nitrate and piperidine in the gastro-intestinal tract of the rat. Nature 232, 199–200.
- Macfarlane, S. and Macfarlane, G.T. (2006) Composition and metabolic activities of bacterial biofilms colonizing food residues in the human gut. Appl. Environ. Microbiol. 72, 6204–6211.
- Belcheva, A. et al. (2014) Gut microbial metabolism drives transformation of MSH2-deficient colon epithelial cells. Cell 158, 288–299.
- Chaturvedi, R. et al. (2011) Spermine oxidase mediates the gastric cancer risk associated with Helicobacter pylori CagA. Gastroenterology 141, 1696–1708.
- Babbar, N. and Casero, R.A., Jr (2006) Tumor necrosis factor-alpha increases reactive oxygen species by inducing spermine oxidase in human lung epithelial cells: a potential mechanism for inflammation- induced carcinogenesis. Cancer Res. 66, 11125–11130.
- Tucker, J.M. et al. (2005) Potent modulation of intestinal tumorigenesis in ApcMin/+ mice by the polyamine catabolic enzyme spermidine/ spermine N1-acetyltransferase. Cancer Res. 65, 5390–5398.
- Li, Y. et al. (2012) IL-6-induced DNMT1 activity mediates SOCS3 promoter hypermethylation in ulcerative colitis-related colorectal cancer. Carcinogenesis 33, 1889–1896.
- Meira, L.B. et al. (2008) DNA damage induced by chronic inflammation contributes to colon carcinogenesis in mice. J. Clin. Invest. 118, 2516–2525.
- Wang, L. et al. (2009) IL-17 can promote tumor growth through an IL-6–Stat3 signaling pathway. J. Exp. Med. 206, 1457–1464.
- Grivennikov, S. et al. (2009) IL-6 and Stat3 are required for survival of intestinal epithelial cells and development of colitis-associated cancer. Cancer Cell 15, 103–113.
- Swidsinski, A. et al. (2002) Mucosal flora in inflammatory bowel disease. Gastroenterology 122, 44–54.
- Golinska, E. et al. (2013) Virulence factors of Enterococcus strains isolated from patients with inflammatory bowel disease. World J. Gastroenterol. 19, 3562–3572.
- Gallo, P.M. et al. (2015) Amyloid–DNA composites of bacterial biofilms stimulate autoimmunity. Immunity 42, 1171–1184.
- Oppong, G.O. et al. (2015) Biofilm-associated bacterial amyloids dampen inflammation in the gut: oral treatment with curli fibres reduces the severity of hapten-induced colitis in mice. NPJ Bio- films Microbiomes 1, 15019.
- Nishimori, J.H. et al. (2012) Microbial amyloids induce interleukin 17A (IL-17A) and IL-22 responses via Toll-like receptor 2 activation in the intestinal mucosa. Infect. Immun. 80, 4398–4408.
- Oppong, G.O. et al. (2013) Epithelial cells augment barrier function via activation of the Toll-like receptor 2/phosphatidylinositol 3- kinase pathway upon recognition of Salmonella enterica serovar Typhimurium curli fibrils in the gut. Infect. Immun. 81, 478–486.
- Rapsinski, G.J. et al. (2015) Toll-like receptor 2 and NLRP3 cooperate to recognize a functional bacterial amyloid, curli. Infect. Immun. 83, 693–701.
- Nitsche, U. et al. (2016) Right sided colon cancer as a distinct histopathological subtype with reduced prognosis. Dig. Surg. 33, 157–163.





